Generalidad
Amiloidosis es el término utilizado para definir un grupo de enfermedades caracterizadas por la acumulación, a menudo en el área extracelular, de un material proteico fibrilar, definido como amiloide, las fibrillas amiloides insolubles forman depósitos particularmente estables en numerosos órganos.

Otras fotos Amiloidosis - Galería 2
Los síntomas y la gravedad de la enfermedad dependen del órgano predominantemente afectado por la acumulación de amiloide y del tipo de amiloidosis. Sin embargo, la mayoría de los casos son sistémicos. En otras palabras, los depósitos fibrilares están muy extendidos y pueden afectar potencialmente el funcionamiento de muchos tejidos y órganos del cuerpo. . El diagnóstico se define por biopsia, al examinar una pequeña muestra de tejido bajo un microscopio. Los factores etiológicos potenciales varían según la variante de amiloidosis. Los tratamientos disponibles pueden ayudar a controlar los síntomas y limitar la producción de amiloide.
Características de los depósitos de amiloide
La amiloidosis se deriva de trastornos de la estructura secundaria de las proteínas (con configuración de hoja plegada en β). En condiciones normales, de hecho, las proteínas se sintetizan en una cadena lineal de aminoácidos que, al plegarse, adquiere una conformación espacial específica. (plegamiento proteico). Gracias a su estructura, por tanto al correcto plegamiento proteico, la proteína es capaz de realizar las funciones fisiológicas de las que es responsable. Las proteínas amiloides derivan de un precursor procesado incorrectamente por las células (debido a un "plegamiento incorrecto "). Las proteínas que forman las fibrillas se diversifican según el tamaño, la secuencia de aminoácidos y la estructura nativa, pero se convierten en agregados insolubles que son similares en estructura y propiedades. Los precursores de las fibrillas están representados por moléculas primarias (ejemplo: cadena ligera de inmunoglobulinas, β2-microglobulina, apolipoproteína A1, etc.) o de productos que reflejen una alteración en la s secuencia de aminoácidos. La estructura secundaria aberrante predispone a la formación de fibrillas, que pueden depositarse localmente en tejidos y órganos y provocar el deterioro de su función fisiológica normal. Se han identificado más de 20 precursores de proteínas diferentes que pueden adquirir una conformación amiloide, que es por qué existen muchos tipos diferentes de amiloidosis.
Según la ubicación de los depósitos de amiloide, la enfermedad se puede dividir en:
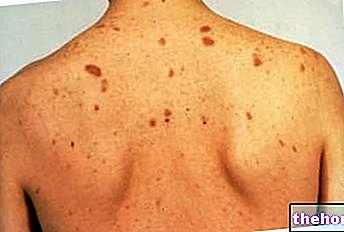
- Forma localizada: confinada a un órgano o tejido en particular (corazón, riñones, tracto gastrointestinal, sistema nervioso y dermis) y suele ser menos grave que las formas sistémicas (difusas). Por ejemplo, la amiloidosis solo puede afectar la piel, causando decoloración y / o picazón. También se ha encontrado un tipo particular de proteína amiloide en el cerebro de pacientes con enfermedad de Alzheimer. La amiloidosis localizada es típica de la senescencia y los pacientes afectados. De diabetes tipo 2 (donde la proteína se acumula en el páncreas).
- Forma sistémica: los depósitos de amiloide están presentes en diversos órganos y generalmente reconocen origen neoplásico, inflamatorio, genético o iatrogénico. La amiloidosis sistémica suele ser muy grave: comúnmente daña el corazón, riñones, intestinos y nervios, provocando insuficiencia progresiva d "órgano".
Clasificación
Existen muchas formas de amiloidosis, clasificadas según la naturaleza de las proteínas que forman los depósitos fibrilares.
Las variantes más comunes son:
- Amiloidosis primaria (también llamada amiloidosis de cadenas ligeras, AL);
- Amiloidosis secundaria (también llamada amiloidosis adquirida, AA);
- Amiloidosis hereditaria;
- Amiloidosis asociada al envejecimiento (o amiloidosis sistémica senil).

.jpg)





















.jpg)
.jpg)
