Esta vía metabólica que involucra varias fases: el colesterol se transfiere de los tejidos periféricos al hígado primero a través del sistema linfático, luego a través del torrente sanguíneo. Los principales componentes que intervienen en el transporte inverso del colesterol son HDL, ABCA1 y apo A-I.
las células periféricas no intestinales o hepáticas son incapaces de degradar el exceso de colesterol; por tanto, para mantener la homeostasis celular, es fundamental la presencia de un mecanismo dedicado a la eliminación del colesterol.
Este mecanismo dirigido a la recuperación hepática del exceso de colesterol periférico se denomina "transporte inverso de colesterol" (ECA: transporte inverso de colesterol).
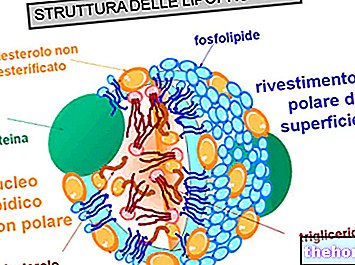
(fosfolípidos y colesterol) que conduce al ensamblaje y generación de partículas HDL maduras.Precursores de HDL
La primera etapa del transporte inverso de colesterol consiste en la producción, por el intestino y el hígado, de precursores discoides de HDL que exponen en su superficie apoproteínas (principalmente ApoA-I).
Así, se liberan moléculas precursoras de HDL denominadas pre-B-HDL, que incorporan cantidades muy pequeñas de colesterol y lípidos, especialmente fosfolípidos. La presencia de estas moléculas precursoras a nivel periférico promueve la transferencia del exceso de colesterol libre (FC), filtrado de las células de los tejidos periféricos, a la apo AI, mediante la intervención de un transportador de membrana llamado casete de unión a ATP A1 (ABCA1).
Este transportador se localiza en la superficie celular y en las membranas de Golgi, y puede transportar lípidos desde el aparato de Golgi a la membrana celular, facilitando así su salida.
En este punto, tan pronto como el colesterol libre entra en la HDL nativa, interviene una enzima plasmática de origen hepático, denominada lecitina-colesterol aciltransferasa plasmática o más simplemente LCAT; esta enzima convierte el colesterol libre incorporado en el pre-B-HDL en ésteres de colesterol, transformando el pre-B-HDL en su forma madura de α-HDL; en la práctica, la acumulación continua de colesterol en el núcleo de las lipoproteínas convierte las HDL discoidales en partículas esféricas y gruesas, que pueden adquirir además apoproteínas de las partículas de lipoproteínas ricas en triglicéridos y fusionarse entre sí.
En todo el proceso, la apolipoproteína AI juega un papel clave, estimulando tanto la actividad del transportador ABCA1 como la del LCAT. Dado que la ApoAI es la apolipoproteína más representada en las HDL, su concentración plasmática está directamente relacionada con los niveles de colesterol HDL.
TENGA EN CUENTA: el proceso de esterificación es esencial para evitar la redifusión del colesterol de HDL a la membrana plasmática; este mecanismo aprovecha el ácido graso en la posición dos presente en las moléculas de fosfatidilcolina.
El proceso de esterificación mediado por LCAT luego transforma las moléculas de pre-B-HDL en su forma esférica de α-HDL "madura". Estas lipoproteínas luego se transportan al hígado, donde liberan colesterol, de acuerdo con dos vías distintas.
Primera vía hepática
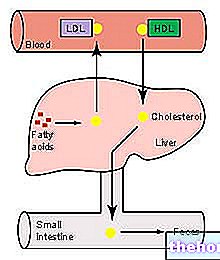
En el primer caso, las HDL ricas en colesterol esterificado transfieren este lípido a las lipoproteínas ricas en triglicéridos (lipoproteínas de muy baja y baja densidad), que luego son interceptadas por el hígado a través de receptores específicos (LDL-R) y retiradas de la circulación.
El objetivo es transportar el colesterol periférico al hígado a través del sistema receptor de LDL, luego "descargar" el HDL del exceso de colesterol a nivel periférico, para que estén disponibles nuevamente para aceptarlo de los tejidos; Al agotar el colesterol, las HDL aceptan triglicéridos a cambio y esto sucede gracias a la proteína de transferencia de ésteres de colesterol (CETP).
La función de esta proteína es, por tanto, favorecer la redistribución y equilibrio de los ésteres de colesterol y triglicéridos entre las lipoproteínas HDL, LDL, IDL, VLDL, quilomicrones y restos de quilomicrones, conduciendo, como resultado neto, a un enriquecimiento en triglicéridos de HDL, a expensas de los ésteres de colesterol y una reducción del tamaño de las HDL.
Segunda ruta del hígado
La segunda vía involucra receptores SR-B1 hepáticos para HDL ricos en colesterol esterificado, en ausencia de degradación concomitante de la porción proteica de HDL, que luego se recicla. En la práctica, esta enzima permite vaciar el contenido de HDL y regenerar nuevas pre-B-HDL.
Sin embargo, parte de HDL y ApoA-I se internaliza y degrada a nivel lisosomal, tanto en las células hepáticas como en las renales. La captación mediada por SR-B1 se hace más eficiente por la actividad de la lipasa hepática, capaz de remodelar HDL hidrolizando los fosfolípidos superficiales y permitiendo el flujo de colesterol esterificado desde el núcleo de lipoproteínas hacia la membrana plasmática (se hipotetiza, entre "otros , que la ApoE también participa en la captación selectiva, ya que los ratones deficientes en el gen ApoE muestran una reducción en la eficacia de esta vía). SR-BI se expresa principalmente en el hígado, las glándulas suprarrenales y el ovario.