¿Qué es Rebif?
Rebif es una solución inyectable en jeringas y cartuchos precargados. Las jeringas contienen 8,8, 22 o 44 microgramos del principio activo interferón beta-1a. Los cartuchos contienen un total de 66 o 132 microgramos de interferón beta-1a y están diseñados para dosis múltiples a través de un inyector electrónico que administra 8,8, 22 o 44 microgramos por dosis.
¿Para qué se utiliza Rebif?
Rebif está indicado para el tratamiento de la esclerosis múltiple (EM) recidivante. Es un tipo de esclerosis múltiple en la que el paciente sufre ataques (recaídas), seguidos de períodos libres de síntomas. No se ha demostrado que el medicamento sea eficaz en pacientes con EM secundaria progresiva (EM que se produce después de EM con recaídas) en ausencia de exacerbaciones. Rebif no debe utilizarse en niños menores de 12 años debido a la falta de información sobre su uso. de la medicina en esta población.
La medicina solo se puede obtener con una receta.
¿Cómo se usa Rebif?
El tratamiento con Rebif debe iniciarse bajo la supervisión de un médico con experiencia en el tratamiento de la EM. La dosis recomendada de Rebif es de 44 microgramos tres veces por semana mediante inyección subcutánea (debajo de la piel). La dosis de 22 microgramos se recomienda para pacientes que no pueden tolerar la dosis más alta y para adolescentes de 12 a 16 años.
Al iniciar el tratamiento con Rebif por primera vez, la dosis debe aumentarse gradualmente para evitar reacciones adversas, comenzando con 8,8 microgramos tres veces por semana durante las dos primeras semanas y luego continuando con 22 microgramos tres veces por semana durante las siguientes dos semanas. semanas. Se encuentran disponibles envases especiales con el número correcto de jeringas o cartuchos para iniciar el tratamiento. El inyector electrónico utilizado con los cartuchos está programado para administrar las dosis correctas de Rebif al inicio del tratamiento y durante la fase de dosis estándar.
El paciente puede inyectarse Rebif él mismo si se le ha indicado adecuadamente. El médico puede recomendar al paciente que tome un analgésico antipirético antes de cada inyección y 24 horas después de la inyección para aliviar los síntomas similares a los de la gripe que pueden aparecer como reacción adversa al tratamiento. Todos los pacientes deben ser controlados al menos una vez cada dos años. .
¿Cómo actúa Rebif?
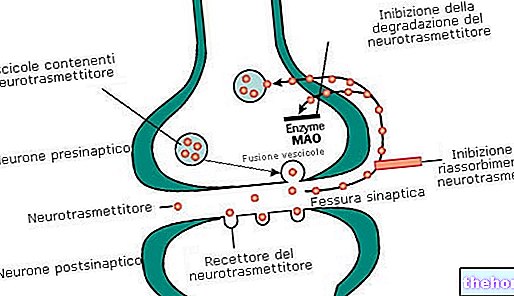
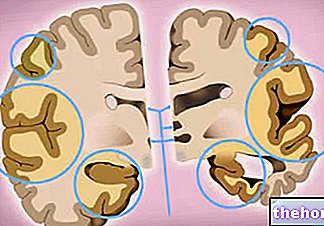
La EM es una enfermedad nerviosa en la que la inflamación destruye la vaina protectora que recubre los nervios. Esto se denomina "desmielinización". El principio activo de Rebif, el interferón beta-1a, pertenece al grupo de los interferones. Los interferones son sustancias. Productos naturales producidos por el cuerpo para ayudarlo a hacer frente a ataques como las infecciones virales. El mecanismo de acción de Rebif en la EM aún no se comprende por completo, pero el interferón beta parece calmar el sistema inmunológico y prevenir la recurrencia de la EM.
El interferón beta-1a se produce mediante un método conocido como "técnica del ADN recombinante": se elabora a partir de una célula que se ha insertado en un gen (ADN) que le permite producir interferón beta-1a. El análogo del interferón beta-1a actúa de la misma forma que el interferón beta natural.
¿Qué tipo de estudios se han realizado con Rebif?
Rebif se ha estudiado en 560 pacientes con EM en recaída. Los pacientes habían experimentado al menos dos recaídas en los 2 años anteriores. Los pacientes fueron tratados con Rebif (22 o 44 microgramos) o placebo (un tratamiento ficticio) durante dos años. Posteriormente, el estudio se amplió a cuatro años.
El número de recaídas de pacientes se consideró como la principal medida de eficacia.
Rebif también se ha estudiado en pacientes con EM secundaria progresiva. Este estudio evaluó la eficacia del fármaco para prevenir la progresión de la discapacidad durante tres años.
La empresa no ha realizado estudios formales en pacientes menores de 16 años. Sin embargo, presentó información de estudios publicados sobre el uso de Rebif en adolescentes de 12 a 18 años.
¿Qué beneficio ha demostrado tener Rebif durante los estudios?
Rebif fue más eficaz que el placebo para reducir el número de recaídas de EM remitente-recurrente. La recaída disminuyó aproximadamente un 30% durante dos años con Rebif 22 microgramos y Rebif 44 microgramos en comparación con placebo, y en un 22% (Rebif 22 microgramos) y un 29% (Rebif 44 microgramos) durante cuatro años.
En el estudio en pacientes con EM progresiva, no se observó ningún efecto significativo sobre la progresión de la discapacidad, pero la tasa de recaída disminuyó en aproximadamente un 30%. Se observaron algunos efectos sobre la progresión de la discapacidad solo en pacientes que habían informado recaídas en los dos años anteriores al inicio del estudio.
Los estudios publicados han mostrado una disminución en la tasa de recaída en pacientes de 12 a 18 años. Esta disminución puede estar relacionada con el tratamiento con Rebif.
¿Cuál es el riesgo asociado a Rebif?
Los efectos secundarios más frecuentes (observados en más de 1 de cada 10 pacientes) con Rebif son síntomas similares a los de la gripe, neutropenia, linfopenia y leucopenia (número reducido de glóbulos blancos), trombocitopenia (número reducido de plaquetas), anemia (número reducido de glóbulos blancos). rojo), dolor de cabeza, inflamación y otras reacciones en el lugar de la inyección, así como aumento de las transaminasas (enzimas hepáticas) Se han observado efectos secundarios similares en menores.Para obtener la lista completa de efectos secundarios notificados con Rebif, consulte el prospecto.
Rebif no debe administrarse a pacientes con antecedentes de hipersensibilidad (alergia) al interferón beta natural o recombinante oa cualquiera de los demás componentes. El tratamiento con Rebif no debe iniciarse durante el embarazo. Las pacientes que quedan embarazadas durante el tratamiento deben consultar a su médico. , Rebif no debe ser tomado por pacientes con depresión severa o con tendencias suicidas.
¿Por qué se ha aprobado Rebif?
El Comité de Medicamentos de Uso Humano (CHMP) decidió que los beneficios de Rebif son mayores que sus riesgos en el tratamiento de pacientes con EM recidivante y, por tanto, recomendó autorizar su comercialización.
Otras informaciones sobre Rebif:
El 4 de mayo de 1998, la Comisión Europea concedió a Serono Europe Limited una "autorización de comercialización" para Rebif, válida en toda la Unión Europea. La "autorización de comercialización" fue renovada el 4 de mayo de 2003 y el 4 de mayo de 1998. Mayo de 2008.
Para obtener la versión completa del EPAR de Rebif, haga clic aquí.
Última actualización de este resumen: 01-2009
La información sobre Rebif - Interferon beta-1a publicada en esta página puede estar desactualizada o incompleta. Para un uso correcto de esta información, consulte la página de exención de responsabilidad e información útil.