Ingredientes activos: Gabapentina
Gabapentina Pfizer 600 mg comprimidos recubiertos con película.
Gabapentina Pfizer 800 mg comprimidos recubiertos con película.
Los prospectos de Gabapentina - Medicamento genérico están disponibles para tamaños de envase: - Gabapentina Pfizer 600 mg comprimidos recubiertos con película.
Gabapentina Pfizer 800 mg comprimidos recubiertos con película. - Gabapentina Pfizer 100 mg cápsulas duras, Gabapentina Pfizer 300 mg cápsulas duras, Gabapentina Pfizer 400 mg cápsulas duras
¿Por qué se utiliza gabapentina - fármaco genérico? ¿Para qué sirve?
Gabapentina Pfizer pertenece a un grupo de medicamentos que se utilizan para tratar la epilepsia y el dolor neuropático periférico (dolor prolongado causado por daños en los nervios). El principio activo de Gabapentina Pfizer es gabapentina.
Gabapentin Pfizer se usa para tratar:
- Varias formas de epilepsia (convulsiones inicialmente limitadas a ciertas áreas del cerebro, ya sea que las convulsiones se diseminen a otras partes del cerebro o no). Su médico le recetará Gabapentina Pfizer para ayudarlo a tratar la epilepsia cuando el tratamiento que ya está tomando no controle completamente su condición. Debe tomar Gabapentina Pfizer además de su tratamiento existente a menos que reciba otras instrucciones. Gabapentina Pfizer también puede usarse sola para tratar a adultos y niños mayores de 12 años.
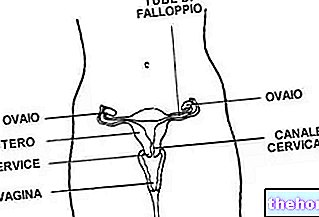
- Dolor neuropático periférico (dolor prolongado causado por daño a los nervios). Una variedad de enfermedades diferentes pueden causar dolor neuropático periférico (ocurre principalmente en las piernas y / o los brazos), como la diabetes o el herpes zóster. Las sensaciones de dolor pueden describirse como calor, ardor, pulsaciones, dolores de rayo, punzantes, dolores agudos, calambres. , dolor, hormigueo, entumecimiento, dolores punzantes, etc.
Contraindicaciones cuando no se debe utilizar gabapentina - fármaco genérico
No tome Gabapentina Pfizer
- si es alérgico (hipersensible) a la gabapentina oa cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
Precauciones de uso Lo que necesita saber antes de tomar Gabapentina - Medicamento genérico
Consulte a su médico o farmacéutico antes de tomar Gabapentina Pfizer:
- Si tiene problemas de riñón, su médico puede recetarle una pauta posológica diferente.
- si está en hemodiálisis (para eliminar los desechos de la insuficiencia renal), informe a su médico si tiene dolor muscular y / o debilidad
- Si desarrolla signos como dolor de estómago persistente, náuseas y vómitos, póngase en contacto con su médico inmediatamente, ya que pueden ser síntomas de pancreatitis aguda (una "inflamación del páncreas).
Se han notificado casos de abuso y dependencia de gabapentina a partir de la experiencia posterior a la comercialización. Informe a su médico si tiene antecedentes de abuso o dependencia.
Un pequeño número de pacientes en tratamiento con medicamentos antiepilépticos como gabapentina han desarrollado pensamientos de suicidio o autolesión. Si en algún momento tiene estos pensamientos, comuníquese con su médico de inmediato.
Información importante sobre reacciones potencialmente graves
Un pequeño número de pacientes en tratamiento con Gabapentina Pfizer han tenido una reacción alérgica o una reacción cutánea potencialmente grave que, si no se trata, puede convertirse en problemas más graves. Debe conocer los síntomas para poder reconocerlos mientras esté tomando Gabapentina Pfizer.
Lea la descripción de estos síntomas en la sección 4 de este prospecto en "Póngase en contacto con su médico inmediatamente si nota alguno de los siguientes síntomas después de tomar este medicamento, ya que pueden ser graves".
Debilidad muscular, molestias o dolores y, en particular, si se siente mal y tiene fiebre al mismo tiempo, puede deberse a una rotura muscular que puede poner en peligro la vida y provocar problemas renales. También pueden producirse decoloración de la orina y cambios en los análisis de sangre (especialmente aumento de creatinfosfoquinasa). Si experimenta alguno de estos signos o síntomas, comuníquese con su médico de inmediato.
Interacciones ¿Qué medicamentos o alimentos pueden modificar el efecto de la gabapentina - medicamento genérico?
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o podría tener que tomar cualquier otro medicamento.
Medicamentos que contienen opioides como morfina.
Si está tomando medicamentos que contienen opioides (como morfina), informe a su médico o farmacéutico porque los opioides pueden aumentar el efecto de Gabapentina Pfizer. Además, la combinación de gabapentina con opioides puede causar síntomas como somnolencia y / o disminución de la presión arterial. .respiración.
Antiácidos para una mala digestión
Si se toman juntos gabapentina pfizer y antiácidos que contienen aluminio y magnesio, la absorción de gabapentina pfizer en el estómago puede verse reducida, por lo que se recomienda tomar gabapentina pfizer no antes de dos horas después de tomar el antiácido.
Gabapentina Pfizer:
- no se espera que interactúe con otros medicamentos antiepilépticos o la píldora anticonceptiva.
- puede interferir con algunas pruebas de laboratorio; Si necesita un análisis de orina, informe a su médico o al hospital qué está tomando.
Toma de gabapentina Pfizer con alimentos
Gabapentin Pfizer se puede tomar con o sin alimentos.
Advertencias Es importante saber que:
Embarazo, lactancia y fertilidad
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
El embarazo
No debe tomar gabapentina Pfizer durante el embarazo a menos que su médico le indique lo contrario. Las mujeres en edad fértil deben utilizar un método anticonceptivo eficaz.
No se han realizado estudios específicos para evaluar el uso de gabapentina en mujeres embarazadas, pero se ha informado de un mayor riesgo para el desarrollo del niño con otros medicamentos utilizados para tratar las convulsiones, particularmente cuando se toma más de un medicamento al mismo tiempo. un medicamento para las convulsiones Por lo tanto, siempre que sea posible, debe intentar tomar solo un medicamento para la epilepsia durante el embarazo y solo por consejo médico.
Comuníquese con su médico de inmediato si está embarazada, cree que podría estarlo o tiene intención de quedarse embarazada mientras toma Gabapentina Pfizer. No deje de tomar este medicamento de forma repentina, ya que esto puede provocar una aparición repentina de convulsiones que pueden tener graves consecuencias para usted y su bebé.
Hora de la comida
La gabapentina, el principio activo de Gabapentina Pfizer, pasa a la leche materna. Como se desconoce el efecto sobre el bebé, se recomienda que no amamante durante el tratamiento con Gabapentina Pfizer.
Fertilidad
Los estudios en animales no han mostrado ningún efecto sobre la fertilidad.
Conducción y uso de máquinas
Gabapentin Pfizer puede provocar mareos, somnolencia y cansancio. No debe conducir vehículos, operar maquinaria compleja o participar en otras actividades potencialmente peligrosas hasta que comprenda si este medicamento puede afectar su capacidad para realizar estas actividades.
Dosis, método y momento de administración Cómo usar Gabapentina - Medicamento genérico: Posología
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. Si no está seguro, consulte a su médico o farmacéutico.
Su médico determinará la dosis adecuada para usted.
Epilepsia, la dosis recomendada es:
Adultos y adolescentes:
Tome la cantidad de comprimidos que le haya recetado su médico. Por lo general, su médico aumentará la dosis gradualmente. La dosis inicial generalmente estará entre 300 mg y 900 mg por día. Posteriormente, la dosis puede aumentarse, por recomendación del médico, hasta un máximo de 3600 mg al día y su médico le indicará que tome esta dosis en 3 tomas separadas, es decir, una por la mañana, una por la tarde y otra por la mañana. la noche.
Niños a partir de 6 años:
La dosis que se debe administrar al niño la determinará el médico porque se calcula en función del peso del niño. El tratamiento se inicia con una dosis inicial baja que se aumenta gradualmente durante unos 3 días La dosis habitual para controlar la epilepsia es de 25 a 35 mg / kg al día. Por lo general, se administra en 3 dosis divididas, tomando el (los) comprimido (s) cada día, generalmente una vez por la mañana, una vez por la tarde y una vez por la noche.
No se recomienda el uso de Gabapentin Pfizer en niños menores de 6 años.
Dolor neuropático periférico, la dosis recomendada es:
Adultos:
Tome la cantidad de comprimidos de acuerdo con las instrucciones de su médico. Por lo general, su médico aumentará la dosis gradualmente. La dosis inicial estará generalmente entre 300 mg y 900 mg por día. Posteriormente, la dosis puede aumentarse por recomendación del médico hasta un máximo de 3600 mg por día y su médico le indicará que tome el medicamento dividido en 3 tomas, es decir, una por la mañana, una por la tarde y otra por la noche. .
Si tiene problemas de riñón o está en hemodiálisis.: Si tiene problemas de riñón o está en hemodiálisis, su médico puede recetarle un horario diferente para tomar este medicamento y / o una dosis diferente.
Si es un paciente de edad avanzada (mayor de 65 años), debe tomar su dosis normal de gabapentina pfizer, a menos que tenga problemas renales. Si tiene problemas de riñón, su médico puede recetarle un horario diferente para tomar el medicamento y / o una dosis diferente.
Si estima que el efecto de Gabapentina Pfizer es demasiado fuerte o demasiado débil, informe a su médico o farmacéutico lo antes posible.
Método de administración:
Uso oral.
Trague siempre los comprimidos con una gran cantidad de agua. El comprimido se puede dividir en mitades iguales.
Continúe el tratamiento con Gabapentina Pfizer hasta que su médico le diga que deje de
Sobredosis Qué hacer si ha tomado una sobredosis de Gabapentin - Medicamento genérico
Si toma más Gabapentina Pfizer del que debiera
Una dosis superior a la recomendada puede provocar un aumento de los efectos secundarios, como pérdida del conocimiento, mareos, visión doble, dificultad para hablar, somnolencia y diarrea.
Comuníquese con su médico de inmediato o acuda al servicio de urgencias más cercano si toma más Gabapentina Pfizer de la recetada por su médico. Lleve los comprimidos que no tomó junto con el envase y el prospecto para que el hospital pueda entender fácilmente la cantidad de medicamento que ha tomado.
Si olvidó tomar Gabapentina Pfizer
Si olvidó tomar una dosis, tómela tan pronto como se acuerde, a menos que sea el momento de su próxima dosis. No tome una dosis doble para compensar las dosis olvidadas.
Si interrumpe el tratamiento con Gabapentina Pfizer
No deje de tomar Gabapentina Pfizer a menos que su médico se lo indique. La retirada del tratamiento debe realizarse de forma gradual durante un período de al menos 1 semana. Si deja de tomar Gabapentina Pfizer repentinamente o antes de que su médico se lo recete, aumenta el riesgo de convulsiones.
Si tiene más preguntas sobre el uso de este medicamento, consulte a su médico o farmacéutico.
Efectos secundarios ¿Cuáles son los efectos secundarios de la gabapentina - Medicamento genérico?
Como todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Póngase en contacto con su médico inmediatamente si nota alguno de los siguientes síntomas después de tomar este medicamento, ya que pueden ser graves:
- reacciones cutáneas graves que requieren atención inmediata, hinchazón de los labios y la cara, erupción y enrojecimiento de la piel y / o caída del cabello (estos pueden ser síntomas de una reacción alérgica grave).
- dolor de estómago persistente, náuseas y vómitos, ya que pueden ser síntomas de pancreatitis aguda (una inflamación del páncreas).
- Gabapentin Pfizer puede causar reacciones alérgicas graves o potencialmente mortales, que pueden afectar su piel u otras partes del cuerpo como el hígado o las células sanguíneas. Existe la posibilidad o no de que se produzca una erupción cuando se produce este tipo de reacción. Esto puede provocar su hospitalización o la interrupción del tratamiento con gabapentina Pfizer. Comuníquese con su médico de inmediato si tiene alguno de los siguientes síntomas:
- sarpullido
- urticaria
- fiebre
- glándulas agrandadas que persisten o hinchazón de los labios y la lengua
- coloración amarillenta de la piel o el blanco de los ojos
- sangrado inusual
- magulladuras
- fatiga severa o debilidad
- dolor muscular inesperado
- infecciones frecuentes
Estos síntomas pueden ser los primeros signos de una reacción grave. Su médico debe examinarlo para decidir si debe continuar el tratamiento con Gabapentina Pfizer.
Si está en hemodiálisis, informe a su médico si experimenta dolor y / o debilidad muscular.
Otros efectos secundarios incluyen:
Muy frecuentes (pueden afectar a más de 1 de cada 10 personas):
- Infecciones virales
- Sensación de sueño, mareos, falta de coordinación.
- Sensación de cansancio, fiebre.
Frecuentes (pueden afectar hasta 1 de cada 10 personas):
- Neumonía, infecciones respiratorias, infecciones del tracto urinario, inflamación del oído u otras infecciones
- Recuento bajo de glóbulos blancos
- Anorexia, aumento del apetito
- Ira hacia otras personas, confusión, cambios de humor, depresión, ansiedad, nerviosismo, dificultad para pensar
- Convulsiones, movimientos espasmódicos, dificultad para hablar, pérdida de memoria, temblores, alteraciones del sueño, dolores de cabeza, sensibilidad cutánea, disminución de la sensibilidad (entumecimiento), dificultad en la coordinación, movimiento anormal de los ojos, aumento, disminución o ausencia de reflejos.
- Visión borrosa, visión doble.
- Mareo
- Presión arterial alta, enrojecimiento de la cara o dilatación de los vasos sanguíneos.
- Dificultad para respirar, bronquitis, dolor de garganta, tos, nariz seca
- Vómitos, náuseas, problemas dentales, dolor de encías, diarrea, dolor de estómago, indigestión, estreñimiento, sequedad de boca o garganta, flatulencia.
- Hinchazón facial, hematomas, erupción cutánea, picor, acné
- Dolor en las articulaciones, dolor muscular, dolor de espalda, espasmos musculares
- Problemas de erección (impotencia)
- Hinchazón de piernas y brazos, dificultad para caminar, debilidad, dolor, malestar, síntomas similares a los de la gripe.
- Reducción de glóbulos blancos, aumento de peso.
- Heridas accidentales, fracturas, abrasiones Además, en los ensayos clínicos en niños se informaron con frecuencia comportamientos agresivos y movimientos espasmódicos.
Poco frecuentes (pueden afectar hasta 1 de cada 100 personas):
- Reacción alérgica como urticaria
- Reducción de movimiento
- Aumento de la frecuencia cardíaca
- Hinchazón que puede afectar la cara, el tronco y las extremidades.
- Valores anormales de los análisis de sangre que sugieren problemas hepáticos.
- Discapacidad mental
- Caídas
- Aumento de los niveles de glucosa en sangre (visto con más frecuencia en pacientes con diabetes).
Raras (pueden afectar hasta 1 de cada 1.000 personas):
- Pérdida de consciencia
- Disminución de los niveles de glucosa en sangre (observado con más frecuencia en pacientes con diabetes)
Se han notificado las siguientes reacciones adversas desde la fase de poscomercialización de Gabapentina Pfizer:
- Reducción de plaquetas (células que coagulan la sangre).
- Alucinaciones
- Problemas con movimientos anormales como temblores convulsivos, movimientos espasmódicos y rigidez.
- Tintineé en mi oído
- Algunos efectos secundarios, como inflamación de los ganglios linfáticos (pequeños bultos aislados debajo de la piel), fiebre, sarpullido e inflamación del hígado, pueden ocurrir simultáneamente.
- Coloración amarillenta de la piel y los ojos (ictericia). Inflamación del hígado.
- Insuficiencia renal aguda, incontinencia.
- Agrandamiento del tejido mamario, agrandamiento de los senos.
- Eventos adversos que ocurren después de la suspensión brusca de gabapentina (ansiedad, alteraciones del sueño, náuseas, dolor, sudoración), dolor en el pecho.
- Lesión de las fibras musculares (rabdomiólisis).
- Anormalidades en los análisis de sangre (aumento de la creatinfosfoquinasa).
- Problemas con la función sexual, incluida la imposibilidad de alcanzar el orgasmo, eyaculación retardada.
Notificación de efectos secundarios
Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluidos los posibles efectos adversos que no aparecen en este prospecto. Los efectos indeseables también pueden notificarse directamente a través del sistema nacional de notificación en la dirección https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse
Al informar los efectos secundarios, puede ayudar a proporcionar más información sobre la seguridad de este medicamento.
Caducidad y retención
Mantenga este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja y el blister después de CAD. La fecha de vencimiento se refiere al último día de ese mes.
No conservar por encima de 25 ° C.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita, ya que esto ayudará a proteger el medio ambiente.
Composición de Gabapentina Pfizer
El ingrediente activo es gabapentina. Cada comprimido recubierto con película contiene 600 mg u 800 mg de gabapentina.
Los demás componentes de Gabapentina Pfizer comprimidos recubiertos con película son:
poloxámero 407 (óxido de etileno y óxido de propileno)
copovidona
maicena
estearato de magnesio
Película de revestimiento:
blanco opadry YS-1-18111
talco de hidroxipropilcelulosa
Aspecto de Gabapentina Pfizer y contenido del envase
Comprimidos recubiertos con película
Los comprimidos de 600 mg son comprimidos recubiertos con película de color blanco, ovalados, con una línea bisectriz en ambos lados y grabados con "NT" y "16" en un lado.
Los comprimidos de 800 mg son comprimidos recubiertos con película de color blanco, ovalados, con una línea bisectriz en ambos lados y grabados con "NT" y "26" en un lado.
La tableta se puede dividir en mitades iguales.
Blísteres de PVC / PE / PVDC / aluminio o blísteres de PVC / PVDC / aluminio de 20, 30, 45, 50, 60, 84, 90, 100, 200, 500 comprimidos.
Es posible que no se comercialicen todos los tamaños de envases.
Prospecto fuente: AIFA (Agencia Italiana de Medicamentos). Contenido publicado en enero de 2016. Es posible que la información presente no esté actualizada.
Para tener acceso a la versión más actualizada, es recomendable acceder al sitio web de la AIFA (Agencia Italiana de Medicamentos). Descargo de responsabilidad e información útil.
01.0 NOMBRE DEL MEDICAMENTO
GABAPENTIN PFIZER
02.0 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada comprimido recubierto con película contiene 600 mg de gabapentina.
Cada comprimido recubierto con película contiene 800 mg de gabapentina.
Para consultar la lista completa de excipientes, ver sección 6.1.
03.0 FORMA FARMACÉUTICA
Comprimido recubierto con película
Los comprimidos recubiertos con película de Gabapentina Pfizer 600 mg son comprimidos recubiertos con película ovalados, blancos (largo y ancho: 8,96 x 17,27 mm, grosor: 6,48 mm) con una línea bisectriz en ambos lados e impresos con "NT" y "16" en por un lado.
Los comprimidos recubiertos con película de Gabapentina Pfizer 800 mg son comprimidos recubiertos con película ovalados, blancos (largo y ancho: 9,87 x 19,01 mm; grosor: 7,24 mm) con una línea bisectriz en ambos lados e impresos con "NT" y "26" en por un lado.
La tableta se puede dividir en mitades iguales.
04.0 INFORMACIÓN CLÍNICA
04.1 Indicaciones terapéuticas
Epilepsia:
La gabapentina está indicada como terapia complementaria en el tratamiento de las crisis parciales en presencia o ausencia de generalización secundaria en adultos y niños a partir de los 6 años (ver sección 5.1).
La gabapentina está indicada como monoterapia para el tratamiento de las convulsiones parciales en presencia o ausencia de generalización secundaria en adultos y adolescentes a partir de los 12 años de edad.
Tratamiento del dolor neuropático periférico:
La gabapentina está indicada en adultos para el tratamiento del dolor neuropático periférico, como la neuropatía diabética dolorosa y la neuralgia postherpética.
04.2 Posología y forma de administración
La Tabla 1 describe el esquema de titulación para iniciar el tratamiento para todas las indicaciones; Este régimen de dosificación se recomienda tanto en adultos como en adolescentes de 12 años o más. Las instrucciones de dosificación para su uso en niños menores de 12 años se proporcionan en un subcapítulo separado más adelante en esta sección.
Tabla 1 ESQUEMA DE DOSIFICACIÓN - TITULACIÓN INICIAL
Interrupción de la gabapentina:
De acuerdo con la práctica clínica actual, si se debe suspender el tratamiento con gabapentina, se recomienda hacerlo gradualmente al menos durante una semana, independientemente de la indicación que se esté tratando.
Epilepsia:
La epilepsia generalmente requiere tratamientos a largo plazo, la dosis la establece el médico tratante sobre la base de la tolerabilidad y eficacia para el paciente individual.
Adultos y adolescentes:
En los ensayos clínicos, el rango de dosis efectivo fue de 900 a 3600 mg / día. El tratamiento se puede iniciar con una titulación de la dosis como se describe en la Tabla 1 o administrando 300 mg tres veces al día (TID) el primer día. respuesta individual del paciente y tolerabilidad, la dosis puede incrementarse en 300 mg / día paso a paso cada 2-3 días hasta un máximo de 3600 mg / día En algunos pacientes puede ser apropiado una titulación más lenta de la dosis de gabapentina. El tiempo mínimo para alcanzar la dosis de 1800 mg / día es de una semana, para la dosis de 2400 mg / día es de 2 semanas y para la de 3600 mg / día es de 3 semanas. ensayos clínicos a plazo abierto. La dosis diaria total debe dividirse en tres administraciones únicas y, para evitar la aparición repentina de convulsiones, el intervalo de tiempo máximo entre dosis no debe exceder las 12 horas.
Niños de 6 años o más:
La dosis inicial debe variar entre 10 y 15 mg / kg / día y la dosis efectiva se logra aumentando la titulación durante un período de aproximadamente tres días. La dosis eficaz de gabapentina en niños de 6 años o más es de 25 a 35 mg / kg / día. Las dosis de hasta 50 mg / kg / día han sido bien toleradas en un estudio clínico a largo plazo La dosis diaria total debe dividirse en tres administraciones únicas y el intervalo de tiempo máximo entre dosis no debe exceder las 12 horas.
No es necesario controlar las concentraciones plasmáticas de gabapentina para optimizar el tratamiento con gabapentina. Además, la gabapentina se puede utilizar en combinación con otros medicamentos antiepilépticos sin riesgo de alterar las concentraciones plasmáticas de gabapentina o las concentraciones séricas de otros medicamentos antiepilépticos.
Dolor neuropático periférico
Adultos:
La terapia se puede iniciar con titulación de la dosis como se describe en la Tabla 1. Alternativamente, la dosis inicial es de 900 mg / día dividida en tres administraciones iguales. A partir de entonces, en función de la respuesta y la tolerabilidad del paciente individual, la dosis puede aumentarse aún más en 300 mg / día a la vez cada 2-3 días hasta un máximo de 3600 mg / día. En algunos pacientes, puede ser apropiado un ajuste más lento de la dosis de gabapentina. El tiempo mínimo para alcanzar la dosis de 1800 mg / día es de una semana, para la dosis de 2400 mg / día es de 2 semanas y para la de 3600 mg / día es de 3 semanas.
En el tratamiento del dolor neuropático periférico, como la neuropatía diabética dolorosa y la neuralgia postherpética, no se han investigado la eficacia y la seguridad en ensayos clínicos para períodos de tratamiento superiores a 5 meses. Si un paciente requiere un tratamiento superior a 5 meses. dolor neuropático periférico, el médico tratante debe evaluar el estado clínico del paciente y determinar la necesidad de prolongar el tratamiento.
Instrucciones para todas las indicaciones:
En pacientes con malas condiciones generales de salud, por ejemplo, pacientes con bajo peso corporal, receptores de trasplantes de órganos, etc., la titulación de la dosis debe realizarse más lentamente, utilizando dosis más bajas o intervalos de tiempo más largos entre incrementos de dosis.
Uso en pacientes de edad avanzada (mayores de 65 años):
Puede ser necesario un ajuste de la dosis en pacientes de edad avanzada debido a la disminución de la función renal relacionada con la edad (ver Tabla 2) La somnolencia, el edema periférico y la astenia pueden ser más frecuentes en los pacientes de edad avanzada.
Uso en pacientes con insuficiencia renal:
En pacientes con insuficiencia renal y / o en aquellos sometidos a hemodiálisis, se recomienda un ajuste de dosis como se describe en la Tabla 2. Las cápsulas de gabapentina 100 mg pueden usarse para seguir las recomendaciones posológicas en pacientes con insuficiencia renal.
Tabla 2 POSOLOGÍA DE Gabapentina EN ADULTOS SEGÚN LA FUNCIONALIDAD RENAL
a La dosis diaria total debe administrarse dividida en tres tomas. Para pacientes con insuficiencia renal (aclaramiento de creatinina
b Administrar en dosis de 300 mg en días alternos.
c Para pacientes con aclaramiento de creatinina
Uso en pacientes sometidos a hemodiálisis:
En pacientes en hemodiálisis con anuria que nunca han sido tratados con gabapentina, se recomienda una dosis de carga de 300 a 400 mg, seguida de una dosis de 200 a 300 mg de gabapentina después de cada sesión de hemodiálisis de 4 horas. En los días libres de hemodiálisis, no se debe administrar el tratamiento con gabapentina.
En pacientes con insuficiencia renal sometidos a hemodiálisis, la dosis de mantenimiento de gabapentina debe basarse en las recomendaciones posológicas enumeradas en la Tabla 2. Además de la dosis de mantenimiento, se recomienda una dosis adicional de 200-300 mg después de cada sesión de hemodiálisis. 4 horas.
Método de administración:
Uso oral.
La gabapentina puede tomarse con o sin alimentos y debe tragarse entera con una cantidad suficiente de líquido (por ejemplo, un vaso de agua).
04.3 Contraindicaciones
Hipersensibilidad al principio activo oa alguno de los excipientes.
04.4 Advertencias especiales y precauciones de uso apropiadas
Se han notificado casos de ideación y comportamiento suicida en pacientes que reciben fármacos antiepilépticos en sus diversas indicaciones. Un metanálisis de ensayos clínicos aleatorizados y controlados con placebo de fármacos antiepilépticos también encontró un pequeño aumento del riesgo de ideación y comportamiento suicidas.
Se desconoce el mecanismo de este riesgo y los datos disponibles no excluyen la posibilidad de un aumento del riesgo con gabapentina.
Por tanto, se debe monitorizar a los pacientes para detectar signos de ideación y comportamiento suicidas y se debe considerar el tratamiento adecuado. Se debe advertir a los pacientes (y cuidadores) que busquen atención médica si surgen signos de ideación o comportamiento suicida.
Si un paciente desarrolla pancreatitis aguda durante el tratamiento con gabapentina, se debe considerar la interrupción del tratamiento con gabapentina (ver sección 4.8).
Aunque no hay evidencia de convulsiones de rebote con gabapentina, la interrupción brusca de los anticonvulsivos en pacientes epilépticos puede empeorar el estado de mal epiléptico (ver sección 4.2).
Con gabapentina, al igual que con otros medicamentos antiepilépticos, algunos pacientes pueden experimentar una mayor frecuencia de convulsiones o el desarrollo de nuevos tipos de convulsiones.
Al igual que con otros antiepilépticos, los intentos de retirar los antiepilépticos concomitantes con gabapentina en pacientes refractarios al tratamiento con más de un fármaco antiepiléptico para lograr la monoterapia con gabapentina tienen una tasa de éxito baja.
La gabapentina no se considera eficaz para tratar los ataques de epilepsia generalizada primaria, como las ausencias y, en algunos pacientes, puede agravar estas convulsiones. Por lo tanto, la gabapentina debe usarse con precaución en pacientes con convulsiones mixtas, incluidas las ausencias.
No se han realizado estudios sistemáticos con gabapentina en pacientes de 65 años o más. En un estudio doble ciego en pacientes con dolor neuropático, se produjo somnolencia, edema periférico y astenia en un porcentaje ligeramente mayor en pacientes de 65 años y mayores que en pacientes más jóvenes. Además de estos datos, las evaluaciones clínicas en este grupo de edad no indican un perfil de eventos adversos diferente al observado en pacientes más jóvenes.
Los efectos de la terapia con gabapentina a largo plazo (más de 36 semanas) sobre el aprendizaje, la inteligencia y el desarrollo en niños y adolescentes no se han estudiado adecuadamente. Por lo tanto, los beneficios de la terapia prolongada deben sopesarse frente a los riesgos potenciales de dicha terapia.
Erupción farmacológica con eosinofilia y síntomas sistémicos (DRESS):
Se han notificado reacciones de hipersensibilidad sistémica graves y potencialmente mortales, como exantema farmacológico con eosinofilia y síntomas sistémicos (DRESS), en pacientes que toman fármacos antiepilépticos, incluida gabapentina (ver sección 4.8).
Es importante tener en cuenta que las manifestaciones tempranas de hipersensibilidad, como fiebre o linfadenopatía, pueden ocurrir incluso si no hay exantema. Si se presentan tales signos o síntomas, se debe examinar al paciente de inmediato. En caso contrario, se debe suspender el tratamiento con gabapentina. es posible establecer una "etiología alternativa para estos signos o síntomas".
Pruebas de laboratorio:
En la determinación semicuantitativa de la proteinuria total con la tira reactiva se pueden obtener resultados falsos positivos. Por lo tanto, se recomienda verificar un resultado positivo obtenido con la prueba de la tira reactiva utilizando métodos basados en un principio analítico diferente, como el método de Biuret, métodos de unión turbidimétrica o colorimétrica, o utilizar estos métodos alternativos desde el principio.
04.5 Interacciones con otros medicamentos y otras formas de interacción
En un estudio en voluntarios sanos (N = 12), cuando se administró una cápsula de morfina de liberación controlada de 60 mg 2 horas antes que una cápsula de gabapentina de 600 mg, el AUC medio de gabapentina aumentó en un 44% en comparación con cuando se administró gabapentina sin morfina. Por lo tanto, se debe vigilar cuidadosamente a los pacientes para detectar cualquier signo de depresión del SNC, como somnolencia, y la dosis de gabapentina o morfina debe reducirse adecuadamente.
No se observaron interacciones entre gabapentina y fenobarbital, fenitoína, ácido valproico o carbamazepina.
La farmacocinética en estado estacionario de gabapentina es similar en sujetos sanos y en pacientes con epilepsia tratados con estos agentes antiepilépticos.
La administración concomitante de gabapentina y anticonceptivos orales que contienen noretindrona y / o etinilestradiol no afecta la farmacocinética en estado estacionario de ninguno de los componentes.
La administración concomitante de gabapentina y antiácidos que contienen aluminio y magnesio reduce la biodisponibilidad de gabapentina hasta en un 24%. Se recomienda que la gabapentina no se tome antes de dos horas después de la administración de los antiácidos.
La excreción renal de gabapentina no se ve afectada por probenecid.
No se espera que la ligera reducción en la excreción renal de gabapentina observada cuando se coadministra con cimetidina sea de importancia clínica.
04.6 Embarazo y lactancia
Riesgo relacionado con la epilepsia y los fármacos antiepilépticos en general:
El riesgo de defectos de nacimiento aumenta 2-3 veces en la descendencia de mujeres tratadas con un medicamento antiepiléptico.Los defectos más frecuentes son labio leporino, malformaciones cardiovasculares y defectos del tubo neural. La terapia con múltiples fármacos antiepilépticos puede estar asociada con un mayor riesgo de malformaciones congénitas que la monoterapia, por lo que es importante usar la monoterapia siempre que sea posible. Las mujeres que puedan quedar embarazadas o que estén en edad fértil deben recibir asesoramiento de un especialista y se debe reevaluar la necesidad de tratamiento antiepiléptico cuando una mujer esté planeando quedarse embarazada. La terapia antiepiléptica no debe interrumpirse repentinamente, ya que puede provocar ataques epilépticos que pueden tener graves consecuencias tanto para la madre como para el bebé. Rara vez se ha observado retraso en el desarrollo en niños nacidos de mujeres epilépticas. No es posible distinguir si el retraso del desarrollo es causado por factores genéticos o sociales, por la epilepsia de la madre o por un tratamiento antiepiléptico.
Riesgo relacionado con la gabapentina:
No existen datos suficientes sobre el uso de gabapentina en mujeres embarazadas.
Los estudios en animales han mostrado toxicidad para la reproducción (ver sección 5.3). Se desconoce el riesgo potencial para los humanos. La gabapentina no debe usarse durante el embarazo a menos que el beneficio potencial para la madre supere claramente el riesgo potencial para el feto.
No es posible sacar conclusiones definitivas sobre la posible asociación entre gabapentina y un mayor riesgo de malformaciones congénitas cuando el fármaco se toma durante el embarazo, debido a la epilepsia en sí y a la presencia de fármacos antiepilépticos utilizados concomitantemente en el curso de embarazos individuales examinados.
La gabapentina se excreta en la leche materna. Debido a que se desconocen los efectos sobre el bebé durante la lactancia, se debe tener precaución cuando se administre gabapentina a mujeres que amamantan. La gabapentina solo debe usarse en madres que amamantan si los beneficios superan claramente los riesgos.
04.7 Efectos sobre la capacidad para conducir y utilizar máquinas
La gabapentina puede tener "una influencia leve o moderada sobre la capacidad para conducir y utilizar máquinas. La gabapentina actúa sobre el sistema nervioso central y puede causar somnolencia, mareos u otros síntomas relacionados. Incluso si han sido de gravedad leve o moderada, estos efectos secundarios pueden puede ser potencialmente peligroso en pacientes que conducen vehículos o utilizan máquinas, especialmente al inicio del tratamiento y después de un aumento de la dosis.
04.8 Efectos indeseables
Las reacciones adversas observadas en los ensayos clínicos en epilepsia (adyuvante y en monoterapia) y dolor neuropático se enumeran a continuación, por clase y por frecuencia: muy frecuentes (> 1/10); común (> 1/100, >1/1.000, > 1/10.000,
Otras reacciones notificadas durante la experiencia postcomercialización se incluyen como una frecuencia "No conocida" (la frecuencia no puede estimarse a partir de los datos disponibles) en cursiva en la lista a continuación.
Dentro de cada grupo de frecuencia, las reacciones adversas se notifican en orden decreciente de gravedad.
Se han notificado casos de pancreatitis aguda durante el tratamiento con gabapentina. La relación causal con gabapentina no está clara (ver sección 4.4).
Se ha informado de miopatía y niveles elevados de creatina quinasa en pacientes sometidos a hemodiálisis debido a insuficiencia renal en etapa terminal.
Las infecciones del tracto respiratorio, la otitis media, las convulsiones y la bronquitis solo se informaron en ensayos clínicos en niños. Además, el comportamiento agresivo y la hipercinesia se informaron con frecuencia en los ensayos clínicos en niños.
04.9 Sobredosis
No se han observado episodios de toxicidad aguda que pongan en peligro la vida con sobredosis de gabapentina hasta dosis de 49 g. Los síntomas de sobredosis incluyeron mareos, visión doble, alteraciones del habla, somnolencia, letargo y diarrea leve. Todos los pacientes se recuperaron por completo con cuidados de apoyo. La absorción reducida de gabapentina en dosis más altas puede limitar la absorción del fármaco en el momento de la sobredosis y, por lo tanto, puede minimizar la toxicidad resultante de las sobredosis.
Las sobredosis de gabapentina, particularmente cuando se asocian con el uso de otros fármacos depresores del SNC, pueden provocar coma.
Aunque la gabapentina puede eliminarse mediante hemodiálisis, la experiencia previa ha demostrado que esto no es necesario. Sin embargo, la hemodiálisis puede estar indicada en pacientes con insuficiencia renal grave.
No se identificó una dosis oral letal de gabapentina en ratones y ratas tratados con dosis de hasta 8000 mg / kg. Los signos de toxicidad aguda en animales incluyeron ataxia, dificultad para respirar, ptosis, hipoactividad o excitación.
05.0 PROPIEDADES FARMACOLÓGICAS
05.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: antiepilépticos; otros antiepilépticos. Código ATC: N03AX12.
Se desconoce el mecanismo de acción exacto de la gabapentina.
La gabapentina está relacionada estructuralmente con el neurotransmisor GABA (ácido gamma-aminobutírico), pero su mecanismo de acción difiere del de muchos otros ingredientes activos que interactúan con las sinapsis GABAérgicas como valproato, barbitúricos, benzodiazepinas, inhibidores de la transaminasa GABA, inhibidores de la captación de GABA. , Agonistas de GABA y profármacos de GABA. Educación in vitro realizado con gabapentina radiomarcada identificó un nuevo sitio de unión de péptidos en los tejidos del cerebro de ratas, incluidos el neocórtex y el hipocampo, que puede estar relacionado con la actividad anticonvulsivante y analgésica de la gabapentina y sus derivados estructurales. El sitio de unión de la gabapentina se identificó como la subunidad alfa2-delta de canales de calcio dependientes de voltaje.
La gabapentina en concentraciones clínicamente relevantes no se une a otros fármacos comunes o receptores de neurotransmisores en el cerebro, incluidos los receptores GABAA, GABAB, benzodiazepina, glutamato, glicina o N-metil-d-aspartato.
La gabapentina no interactúa in vitro con canales de sodio que se diferencian así de la fenitoína y la carbamazepina. La gabapentina reduce parcialmente las respuestas al agonista del glutamato N-metil-d-aspartato (NMDA) en algunos sistemas in vitro, pero solo a concentraciones superiores a 100 mM que no son alcanzables en vivo. La gabapentina reduce ligeramente in vitro la liberación de neurotransmisores monoamínicos. La administración de gabapentina a ratas aumenta el recambio de GABA en numerosas regiones del cerebro de manera similar al valproato de sodio, aunque en diferentes regiones del cerebro. La relevancia de estas diferentes actividades de gabapentina para los efectos anticonvulsivos aún no se ha definido. En los animales, la gabapentina penetra fácilmente en el cerebro y previene las convulsiones por electrochoque máximo, por sustancias convulsivas, incluidos los inhibidores de la síntesis de GABA, y en modelos genéticos de convulsiones.
Un estudio clínico sobre terapia adyuvante en el tratamiento de convulsiones parciales en pacientes pediátricos de 3 a 12 años mostró una diferencia numérica, pero no estadísticamente significativa, en la tasa de respuesta del 50% a favor del grupo de gabapentina en comparación con el grupo de placebo Análisis adicional post-hoc Las tasas de respuesta calculadas sobre la base de la edad no revelaron un efecto estadísticamente significativo de la edad, ni como variable continua ni como variable dicotómica (grupos de edad de 3 a 5 años y de 6 a 12 años). Los datos de este análisis adicional post-hoc se resumen en la siguiente tabla:
* La población intención de tratar modificado se definió como todos los pacientes asignados al azar al fármaco del estudio que también tenían anotaciones de crisis epilépticas evaluables durante 28 días durante las fases inicial y doble ciego.
05.2 "Propiedades farmacocinéticas
Absorción:
Después de la administración oral, las concentraciones plasmáticas máximas de gabapentina se observan en 2-3 horas. La biodisponibilidad de gabapentina (fracción de la dosis absorbida) tiende a disminuir al aumentar la dosis. La biodisponibilidad absoluta de una cápsula de 300 mg es aproximadamente del 60%. Los alimentos, incluida una dieta alta en grasas, no tienen un efecto clínicamente significativo sobre la farmacocinética de gabapentina. .
La farmacocinética de gabapentina no se ve afectada por la administración repetida. Aunque las concentraciones plasmáticas de gabapentina generalmente variaron de 2 mg / mL a 20 mg / mL en estudios clínicos, estas concentraciones no fueron indicativas de seguridad o eficacia. Los parámetros farmacocinéticos se muestran en la Tabla 3.
Tabla 3 - Resumen de los parámetros farmacocinéticos de las concentraciones medias (% CV) de gabapentina en estado estacionario después de la administración cada 8 horas.
Cmax = concentración plasmática máxima en estado estacionario
tmax = Tiempo hasta Cmax
T½ = vida media de eliminación
AUC (0-8) = área bajo la curva en estado estacionario de 0 a 8 horas después de la administración
Ae% = Porcentaje de la dosis del fármaco que se excreta sin cambios en la orina de 0 a 8 horas después de la administración.
NA = No disponible
Distribución:
La gabapentina no se une a las proteínas plasmáticas y tiene un volumen de distribución de 57,7 litros. En pacientes epilépticos, las concentraciones de gabapentina en el líquido cefalorraquídeo (LCR) son aproximadamente el 20% de las concentraciones plasmáticas en estado estacionario correspondientes. La gabapentina está presente en la leche materna de las mujeres lactantes.
Biotransformación:
No hay evidencia de metabolismo de la gabapentina en humanos La gabapentina no induce enzimas hepáticas oxidantes de función mixta responsables del metabolismo de la sustancia.
Eliminación:
La gabapentina se elimina inalterada únicamente por el riñón. La semivida de eliminación de la gabapentina es independiente de la dosis y tiene un promedio de 5-7 horas.
En pacientes de edad avanzada y en pacientes con insuficiencia renal, el aclaramiento plasmático de gabapentina está reducido. La constante de eliminación, el aclaramiento plasmático y el aclaramiento renal de gabapentina son directamente proporcionales al aclaramiento de creatinina.
La gabapentina se elimina del plasma mediante hemodiálisis. Se recomiendan ajustes de dosis en pacientes con insuficiencia renal o en pacientes en hemodiálisis (ver sección 4.2).
La farmacocinética de gabapentina en niños se determinó en 50 sujetos sanos de 1 mes a 12 años. En general, las concentraciones plasmáticas de gabapentina en niños> 5 años fueron comparables a las encontradas en adultos cuando el fármaco se administró en mg / kg. En un estudio farmacocinético realizado en 24 pacientes pediátricos sanos de 1 a 48 meses, se observó una reducción de aproximadamente un 30% en el AUC, una reducción de la Cmax y un aumento del aclaramiento en función del peso. 5 años de edad.
Linealidad / No linealidad:
La biodisponibilidad de gabapentina (fracción de la dosis absorbida) disminuye con el aumento de la dosis y esto confiere no linealidad a los parámetros farmacocinéticos, incluido el parámetro de biodisponibilidad (F), por ejemplo, Ae%, CL / F, Vd / F.Farmacocinética de eliminación (farmacocinética los parámetros que no incluyen parámetros de biodisponibilidad como CLr y T1 / 2) se describen mejor mediante farmacocinética lineal.Las concentraciones plasmáticas de gabapentina en estado estacionario son predecibles a partir de datos de dosis única.
05.3 Datos preclínicos sobre seguridad
Carcinogénesis:
La gabapentina se administró en la dieta a ratones a dosis de 200, 600, 2000 mg / kg / día ya ratas a dosis de 250, 1000, 2000 mg / kg / día durante dos años. Se encontró un aumento estadísticamente significativo en la incidencia de tumores de células acinares pancreáticas solo en ratas macho con la dosis más alta. La concentración plasmática máxima del fármaco en ratas, a una dosis de 2000 mg / kg / día, fue 10 veces mayor. Concentración plasmática elevada en humanos a una dosis de 3600 mg / día. Los tumores de células acinares pancreáticas en ratas macho tienen un bajo grado de malignidad, no afectaron la supervivencia, no dieron como resultado metástasis o invasión de los tejidos circundantes y fueron similares a los observados en animales de control. La relación entre estos tumores de células acinares pancreáticas en la rata macho y el riesgo de cáncer en humanos no está clara.
Mutagénesis:
La gabapentina no tiene potencial genotóxico. No fue mutagénico en pruebas estándar. in vitro realizado con células bacterianas o de mamíferos. La gabapentina no indujo aberraciones estructurales cromosómicas en células de mamíferos in vitro o en vivo y no indujo la formación de micronúcleos en células de médula ósea de hámster.
Fertilidad deteriorada:
No se observaron efectos adversos sobre la fertilidad o la reproducción en ratas a dosis de hasta 2000 mg / kg (aproximadamente cinco veces la dosis diaria máxima en humanos en mg / m2 de superficie corporal).
Teratogénesis:
La gabapentina no aumentó la incidencia de malformaciones, en comparación con los controles, en la descendencia de ratones, ratas o conejos con dosis, respectivamente, de hasta 50, 30 y 25 veces la dosis diaria en humanos de 3600 mg (respectivamente cuatro, cinco u ocho veces la dosis diaria). dosis utilizada en humanos en mg / m2).
La gabapentina provocó un retraso en el proceso de osificación del cráneo, vértebras, miembros anteriores y miembros inferiores en roedores y esto es indicativo de un retraso en el crecimiento fetal. Estos efectos se produjeron en ratones hembra preñados tratados con dosis orales de 1000 o 3000 mg / kg / día durante la organogénesis y en ratas tratadas con dosis de 500, 1000 o 2000 mg / kg antes y durante el apareamiento y durante la gestación. Estas dosis son aproximadamente de 1 a 5 veces la dosis humana de 3600 mg sobre una base de mg / m2.
No se observaron efectos en las hembras preñadas tratadas con 500 mg / kg / día (aproximadamente la mitad de la dosis humana en mg / m2).
Se observó un aumento en la incidencia de hidroureter y / o hidronefrosis en ratas tratadas con 2000 mg / kg / día en un estudio de fertilidad y reproducción general, con 1500 mg / kg / día en un estudio teratológico y respectivamente. 500, 1000 y 2000 mg / kg / día en un estudio perinatal y posnatal. Se desconoce la importancia de estos datos, pero se han asociado con un retraso en el desarrollo. Estas dosis son aproximadamente 1-5 veces la dosis utilizada en el "hombre igual a 3600 mg en un base mg / m2.
En un estudio de teratología realizado en conejos, hubo un aumento en la incidencia de pérdidas fetales posimplantación con dosis de 60, 300 y 1500 mg / kg / día durante la organogénesis. Estas dosis son aproximadamente de ¼ a 8 veces la dosis diaria en humanos de 3600 mg sobre una base de mg / m2.
06.0 INFORMACIÓN FARMACÉUTICA
06.1 Excipientes
Núcleo de la tableta:
Poloxamer 407 (óxido de etileno y óxido de propileno);
copovidona;
maicena;
estearato de magnesio.
Película de revestimiento:
blanco opadry YS-1-18111;
hidroxipropilcelulosa;
talco.
06.2 Incompatibilidad
Irrelevante.
06.3 Período de validez
2 años
06.4 Precauciones especiales de conservación
No conservar por encima de 25 ° C.
06.5 Naturaleza del envase primario y contenido del envase.
Blíster de PVC / PE / PVDC / aluminio o blíster de PVC / PVDC / aluminio
Envases de 20, 30, 45, 50, 60, 84, 90, 100, 200, 500 comprimidos.
Es posible que no se comercialicen todos los tamaños de envases.
06.6 Instrucciones de uso y manipulación
Sin instrucciones especiales.
07.0 TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Pfizer Italia S.r.l. - Via Isonzo, 71 - 04100 Latina
08.0 NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN
"Comprimidos recubiertos con película de 600 mg" 20 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150346 / M
"Comprimidos recubiertos con película de 600 mg" 30 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150359 / M
"Comprimidos recubiertos con película de 600 mg" 45 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150361 / M
"Comprimidos recubiertos con película de 600 mg" 50 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150373 / M
"Comprimidos recubiertos con película de 600 mg" 60 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150385 / M
"Comprimidos recubiertos con película de 600 mg" 84 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150397 / M
"Comprimidos recubiertos con película de 600 mg" 90 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150409 / M
"Comprimidos recubiertos con película de 600 mg" 100 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150411 / M
"Comprimidos recubiertos con película de 600 mg" 200 comprimidos en blíster PVC / PE / PVDC / AL - AIC: 040150423 / M
"Comprimidos recubiertos con película de 600 mg" 500 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150435 / M
"Comprimidos recubiertos con película de 600 mg" 20 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150447 / M
"Comprimidos recubiertos con película de 600 mg" 30 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150450 / M
"Comprimidos recubiertos con película de 600 mg" 45 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150462 / M
"Comprimidos recubiertos con película de 600 mg" 50 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150474 / M
"Comprimidos recubiertos con película de 600 mg" 60 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150486 / M
"Comprimidos recubiertos con película de 600 mg" 84 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150498 / M
"Comprimidos recubiertos con película de 600 mg" 90 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150500 / M
"Comprimidos recubiertos con película de 600 mg" 100 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150512 / M
"Comprimidos recubiertos con película de 600 mg" 200 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150524 / M
"Comprimidos recubiertos con película de 600 mg" 500 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150536 / M
"Comprimidos recubiertos con película de 800 mg" 20 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150548 / M
"Comprimidos recubiertos con película de 800 mg" 30 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150551 / M
"Comprimidos recubiertos con película de 800 mg" 45 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150563 / M
"Comprimidos recubiertos con película de 800 mg" 50 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150575 / M
"Comprimidos recubiertos con película de 800 mg" 60 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150587 / M
"Comprimidos recubiertos con película de 800 mg" 84 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150599 / M
"Comprimidos recubiertos con película de 800 mg" 90 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150601 / M
"Comprimidos recubiertos con película de 800 mg" 100 comprimidos en blíster PVC / PE / PVDC / AL - AIC: 040150613 / M
"Comprimidos recubiertos con película de 800 mg" 200 comprimidos en blíster PVC / PE / PVDC / AL - AIC: 040150625 / M
"Comprimidos recubiertos con película de 800 mg" 500 comprimidos en blíster de PVC / PE / PVDC / AL - AIC: 040150637 / M
"Comprimidos recubiertos con película de 800 mg" 20 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150649 / M
"Comprimidos recubiertos con película de 800 mg" 30 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150652 / M
"Comprimidos recubiertos con película de 800 mg" 45 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150664 / M
"Comprimidos recubiertos con película de 800 mg" 50 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150676 / M
"Comprimidos recubiertos con película de 800 mg" 60 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150688 / M
"Comprimidos recubiertos con película de 800 mg" 84 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150690 / M
"Comprimidos recubiertos con película de 800 mg" 90 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150702 / M
"Comprimidos recubiertos con película de 800 mg" 100 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150714 / M
"Comprimidos recubiertos con película de 800 mg" 200 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150726 / M
"Comprimidos recubiertos con película de 800 mg" 500 comprimidos en blíster de PVC / PVDC / AL - AIC: 040150738 / M
09.0 FECHA DE LA PRIMERA AUTORIZACIÓN O RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de la primera autorización: 02/03/2012
10.0 FECHA DE REVISIÓN DEL TEXTO
Determinación AIFA de 10/06/2013
















.jpg)