Para poder hablar de manera comprensible del "hemoglobina (Hb), conviene ocuparse de la primera mioglobina (Mb) que es muy similar a la hemoglobina pero es mucho más simple. Entre la hemoglobina y la mioglobina existen estrechas relaciones de parentesco: ambas son proteínas conjugadas y su grupo prostético (parte no proteica) es el grupo hemo.
La mioglobina es una proteína globular formada por una sola cadena de unos ciento cincuenta aminoácidos (depende del organismo) y su peso molecular es de unos 18 Kd.
Como se mencionó, está equipado con un grupo hemo que se inserta en una porción hidrófoba (o lipófila) de la proteína, que consiste en pliegues atribuibles a las estructuras de hélice α de las proteínas fibrosas.
La mioglobina está compuesta principalmente por segmentos de hélices α, presentes en número de ocho y consiste, casi exclusivamente, en residuos no polares (leucina, valina, metionina y fenilalanina) mientras que los residuos polares están prácticamente ausentes (ácido aspártico, ácido glutámico, lisina y arginina); los únicos residuos polares son dos histidinas, que juegan un papel fundamental en la unión del oxígeno al grupo hemo.
El grupo hemo es un grupo cromóforo (se absorbe en lo visible) y es el grupo funcional de la mioglobina.
Ver también: hemoglobina glucosilada - hemoglobina en la orina
Un poco de química

El enlace entre la protoporfirina y el hierro es un enlace típico de compuestos de coordinación que son compuestos químicos en los que un átomo central (o ion) forma enlaces con otras especies químicas en un número mayor que su número de oxidación (carga eléctrica). En el caso del hemo, estos enlaces son reversibles y débiles.
El número de coordinación (número de enlaces de coordinación) del hierro es seis: puede haber seis moléculas alrededor del hierro que comparten los electrones de enlace.
Para formar un compuesto de coordinación, se necesitan dos orbitales con la orientación correcta: uno capaz de "adquirir" electrones y el otro capaz de donarlos.
En el hemo, el hierro forma cuatro enlaces planos con los cuatro átomos de nitrógeno en el centro del anillo de protoporfirina y un quinto enlace con un nitrógeno de histidina proximal; el hierro tiene el sexto enlace de coordinación libre y puede unirse al oxígeno.
Cuando el hierro está en forma de ion libre, su tipo orbitales D todos tienen la misma energía; en la mioglobina, el ión de hierro se une a la protoporfirina y la histidina: estas especies perturban magnéticamente los orbitales D algo de hierro el alcance de la perturbación será diferente para los distintos orbitales D dependiendo de su orientación espacial y la de las especies perturbadoras. Dado que la energía total de los orbitales debe ser constante, la perturbación provoca una separación energética entre los distintos orbitales: la energía adquirida por unos orbitales es equivalente a la energía perdida por otros.
Si la separación que se produce entre los orbitales no es muy grande, es preferible una disposición electrónica de alto espín: los electrones de unión intentan organizarse en espines paralelos en tantos subniveles como sea posible (máxima multiplicidad); si, por otro lado, la perturbación es muy fuerte y hay una gran separación entre los orbitales, puede ser más conveniente emparejar los electrones de enlace en los orbitales de menor energía (bajo giro).
Cuando el hierro se une al oxígeno, la molécula asume una disposición de espín bajo, mientras que cuando el hierro tiene el sexto enlace de coordinación libre, la molécula tiene una disposición de espín alto.
Gracias a esta diferencia de espín, a través de un análisis espectral de la mioglobina, podemos entender si el oxígeno (MbO2) está unido a él o no (Mb).
La mioglobina es una proteína muscular típica (pero no se encuentra solo en los músculos).
La mioglobina se extrae del cachalote en el que está presente en grandes cantidades y luego se purifica.
Los cetáceos tienen una respiración como la de los seres humanos: al tener pulmones deben absorber aire a través del proceso respiratorio; el cachalote debe llevar la mayor cantidad de oxígeno posible a los músculos que son capaces de acumular oxígeno al unirlo a la mioglobina presente en ellos; el oxígeno se libera lentamente cuando el cetáceo se sumerge porque su metabolismo requiere oxígeno: cuanto mayor es la cantidad de oxígeno que el cachalote es capaz de absorber y más oxígeno hay disponible durante la inmersión.
La mioglibina se une al oxígeno de manera reversible y está presente en los tejidos periféricos en mayor porcentaje cuanto más se acostumbra ese tejido a trabajar con suministros de oxígeno distantes en el tiempo.
<--- La mioglobina es una proteína presente en los músculos, cuya función es precisamente la de un "reservorio" de oxígeno.
Lo que hace que la carne sea más o menos roja es el contenido de hemoproteínas (es el hemo el que hace que la carne sea roja).
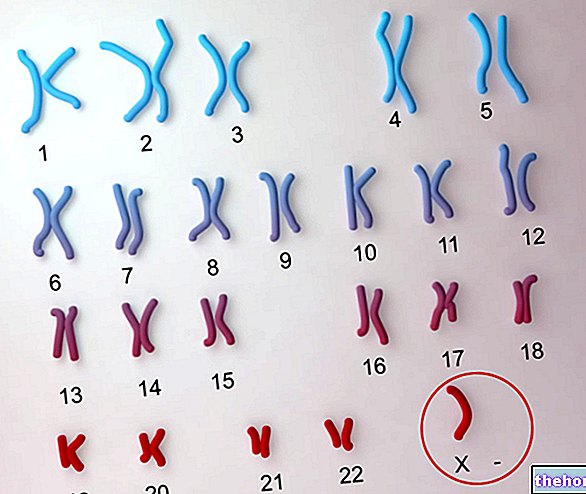
La hemoglobina tiene muchas similitudes estructurales con la mioglobina y es capaz de unirse al oxígeno molecular de forma reversible; pero, mientras que la mioglobina está confinada a los músculos y tejidos periféricos en general, la hemoglobina se encuentra en los eritrocitos o glóbulos rojos (son pseudocélulas, es decir, no son células reales) que constituyen el 40% de la sangre.
A diferencia de la mioglobina, el trabajo de la hemoglobina es tomar oxígeno en los pulmones, liberarlo en las células donde se necesita, tomar dióxido de carbono y liberarlo en los pulmones donde el ciclo comienza nuevamente.
L "hemoglobina es un tetrámetro, es decir, está formado por cuatro cadenas polipeptídicas cada una con un grupo hemo e idénticas de dos en dos (en un ser humano hay dos cadenas alfa y dos cadenas beta).
La función principal de la hemoglobina es el transporte de oxígeno; otra función de la sangre en la que interviene la hemoglobina es el transporte de sustancias a los tejidos.
En el camino de los pulmones (rico en oxígeno) a los tejidos, la hemoglobina transporta oxígeno (al mismo tiempo que las otras sustancias llegan a los tejidos) mientras que en el camino inverso, lleva consigo los desechos recolectados por los tejidos, especialmente el carbono. dióxido producido en el metabolismo.
En el desarrollo de un ser humano existen genes que se expresan solo durante un cierto período de tiempo; por esta razón existen diferentes hemoglobinas: fetal, embrionaria, del hombre adulto.
Las cadenas que componen estas diferentes hemoglobinas tienen diferentes estructuras pero con algunas similitudes, de hecho, la función que realizan es más o menos la misma.
Una explicación de la presencia de varias cadenas diferentes es la siguiente: en el curso del proceso evolutivo de los organismos, incluso la hemoglobina ha evolucionado especializándose en el transporte de oxígeno desde áreas ricas en él hacia áreas deficientes. de la cadena evolutiva l "la hemoglobina transportaba oxígeno en pequeños organismos; en el transcurso de la evolución los organismos alcanzaron mayores dimensiones, por lo que la hemoglobina fue modificada para poder transportar oxígeno a áreas más alejadas del punto donde era rico en él; para Para ello se han codificado, en el transcurso del proceso evolutivo, nuevas estructuras de las cadenas que componen la hemoglobina.
La mioglobina se une al oxígeno incluso a presiones moderadas; en los tejidos periféricos hay una presión (PO2) de unos 30 mmHg: la mioglobina a esta presión no libera oxígeno, por lo que sería ineficaz como transportador de oxígeno. La hemoglobina, en cambio, , tiene un comportamiento más elástico: liga el oxígeno a altas presiones y lo libera cuando la presión disminuye.
Cuando una proteína es funcionalmente activa, puede cambiar un poco su forma; por ejemplo, la mioglobina oxigenada tiene una forma diferente a la mioglobina no oxigenada y esta mutación no afecta a sus vecinas.
La situación es diferente en el caso de proteínas asociadas como la hemoglobina: cuando una cadena se oxigena se induce a cambiar de forma pero esta modificación es tridimensional por lo que las demás cadenas del tetrámetro también se ven afectadas. entre sí., sugiere que la modificación de uno afecta a los demás vecinos aunque en diferente medida; cuando una cadena se oxigena, las otras cadenas del tetrámetro asumen una "actitud menos hostil" hacia el oxígeno: la dificultad con la que una cadena se oxigena disminuye a medida que las cadenas cercanas a él se oxigenan a su vez. Lo mismo ocurre con la desoxigenación.
La estructura cuaternaria de la desoxihemoglobina se llama forma T (tiempo) mientras que la de la oxihemoglobina se llama forma R (liberada); en el estado tenso hay una serie de interacciones electrostáticas bastante fuertes entre los aminoácidos ácidos y los aminoácidos básicos que conducen a una estructura rígida de desoxihemoglobina (por eso la "forma tensa"), mientras que cuando el oxígeno está ligado, la entidad de estos las interacciones disminuyen (de ahí la "forma liberada"). Además, en ausencia de oxígeno, la carga de la histidina (ver estructura) es estabilizada por la carga opuesta del ácido aspártico mientras que, en presencia de oxígeno, existe una tendencia por parte de la proteína a perder un protón; todo esto implica que la hemoglobina oxigenada es un ácido más fuerte que la hemoglobina desoxigenada: efecto bohr.
Dependiendo del pH, el grupo hemo se une más o menos fácilmente al oxígeno: en un ambiente ácido, la hemoglobina libera oxígeno más fácilmente (la forma tensa es estable) mientras que, en un ambiente básico, la unión con el oxígeno es más dura.

Cada hemoglobina libera 0,7 protones por cada mol de oxígeno (O2) que ingresa.
El efecto Bohr permite que la hemoglobina mejore su capacidad para transportar oxígeno.
La hemoglobina que viaja de los pulmones a los tejidos debe equilibrarse en función de la presión, el pH y la temperatura.
Veamos el efecto de la temperatura.
La temperatura en los alvéolos pulmonares es aproximadamente 1-1,5 ° C más baja que la temperatura externa mientras que, en los músculos, la temperatura es aproximadamente 36,5-37 ° C; a medida que aumenta la temperatura, el factor de saturación desciende (a la misma presión): esto sucede porque la energía cinética aumenta y se favorece la disociación.

Hay otros factores que pueden afectar la capacidad de la hemoglobina para unirse al oxígeno, uno de los cuales es la concentración de 2,3 bisfosfoglicerato.
El 2,3 bisfosfoglicerato es un metabólico presente en los eritrocitos en una concentración de 4-5 mM (en ninguna otra parte del organismo está presente en una concentración tan alta).
A pH fisiológico, el 2,3 bisfosfoglicerato está desprotonado y tiene cinco cargas negativas; está encajado entre las dos cadenas beta de la hemoglobina porque estas cadenas tienen una alta concentración de cargas positivas. Las interacciones electrostáticas entre las cadenas beta y el 2,3 bisfosfoglicerato confieren cierta rigidez al sistema: se obtiene una estructura tensa que tiene poca afinidad por el oxígeno, durante la oxigenación se expulsa el 2,3 bisfosfoglicerato.
En los eritrocitos c "hay un aparato especial que convierte el 1,3 bisfosfoglicerato (producido por el metabolismo) en 2,3 bisfosfoglicerato para que alcance una concentración de 4-5 mM y por tanto la hemoglobina sea capaz de intercambiar el" oxígeno en los tejidos ".
La hemoglobina que llega a un tejido está en estado liberado (unida al oxígeno), pero en las proximidades del tejido, se carboxila y pasa al estado tenso: la proteína en este estado tiene menos tendencia a unirse al oxígeno, con respecto al estado liberado, por lo tanto, la hemoglobina libera oxígeno al tejido; además, por reacción entre el agua y el dióxido de carbono, se produce la producción de iones H + y, por lo tanto, más oxígeno debido al efecto bohr.
El dióxido de carbono se difunde en el eritrocito pasando a través de la membrana plasmática; dado que los eritrocitos constituyen aproximadamente el 40% de la sangre, deberíamos esperar que solo el 40% del dióxido de carbono que se difunde de los tejidos ingrese a ellos, de hecho el 90% del dióxido de carbono ingresa a los eritrocitos porque contienen una enzima que convierte el dióxido de carbono en el ácido carbónico, resulta que la concentración estacionaria de dióxido de carbono en los eritrocitos es baja y, por lo tanto, la tasa de entrada es alta.

Otro fenómeno que ocurre cuando un eritrocito llega a un tejido es el siguiente: por gradiente, el "HCO3- (derivado del dióxido de carbono) sale del" eritrocito "y, para equilibrar la salida de una carga negativa, tenemos la" entrada de cloruros que determina un aumento de la presión osmótica: para equilibrar esta variación también se produce la entrada de agua que provoca la hinchazón del eritrocito (efecto HAMBURGER). El fenómeno contrario ocurre cuando un eritrocito llega a los alvéolos pulmonares: un desinflado de los eritrocitos (efecto HALDANE) Por tanto, los eritrocitos venosos (dirigidos a los pulmones) son más redondos que los arteriales.
















-cos-cause-sintomi-e-cura.jpg)