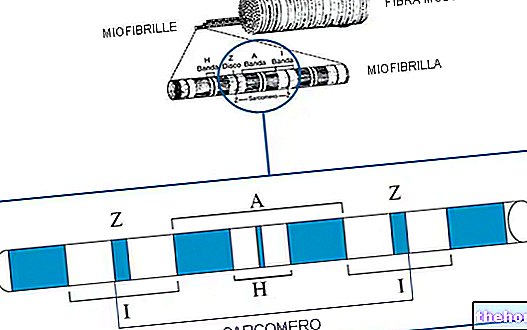
, en primer lugar, implica la modificación estructural de los péptidos denominada desnaturalización de proteínas. Específicamente, la desnaturalización de proteínas significa la distorsión física de las estructuras secundarias, terciarias y cuaternarias de las proteínas, que se produce mediante la ruptura de enlaces estabilizadores (como los puentes disulfuro).

La desnaturalización es un aspecto positivo, de hecho, es el objetivo fundamental para el que es importante cocinar proteínas que, a través de este proceso, pierden su función biológica original y tienden a coagularse, agregarse y perder solubilidad.
La desnaturalización comienza a temperaturas de alrededor de 60-70 ° C y es facilitada por pH ácido (<7) y / o enzimas coagulantes-digestivas.
, como el huevo o la leche, por lo tanto, la liberación de sulfuro de hidrógeno o sulfuro de hidrógeno o sulfuro de dihidrógeno (H2S) se produce como consecuencia de la rotura de los puentes disulfuro.
El H2S es un compuesto tóxico que actúa negativamente sobre las células de todos los tejidos (excepto los glóbulos rojos) ya que inhibe la respiración mitocondrial; obviamente, con solo cocinar los alimentos, la liberación de H2S es mínima y es extremadamente importante. la exactitud de la divulgación, aún debe recordarse.
e implica la diferenciación en cadenas de aminoácidos más pequeñas que son más fácilmente atacadas por los jugos digestivos.y, en ocasiones, (en presencia de oxígeno) determina la oxidación del grupo radical (R). Los aminoácidos más sensibles son: azufrado: cisteína, cistina, metionina (que, como se anticipó, puede liberar sulfuro de hidrógeno) y los heterocíclico: triptófano, tirosina e histidina (el triptófano, en cocción> 200 ° C, puede convertirse en hidrocarburos aromáticos policíclicos).
.
Mecanismo de Maillard: 1) condensación del grupo NH2 de un aminoácido con un carbohidrato y consecuente producción de un base de Shiff; 2) transformación del base de Shiff en un producto de Amadori; 3) transmutación del producto de Amadori en hidrocarburos aromáticos policíclicos, que al cocinarse dan a los alimentos un color marrón y un sabor "cocido", pero también en compuestos intermedios como "hidroximetilfurfural (HMF) o le melanoidinas.
NÓTESE BIEN. Desde el punto de vista nutricional, la reacción de Maillard implica la pérdida parcial del aminoácido lisina y una reducción de la digestibilidad de las melanoidinas por no ser digeribles.
o asar a la parrilla a fuego alto. Finalmente, conviene recordar que la cocción de los alimentos proteicos por excelencia (pescado y carne) es fundamental para prevenir intoxicaciones alimentarias de diversa índole; al respecto ver los artículos: pescado crudo y carne cruda. En cuanto a los huevos y las legumbres, que también son ricas en proteínas, la cocción es importante para inactivar los antinutrientes que podrían dañar el organismo.