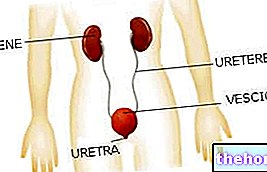
Ingredientes activos: Enalapril (Maleato de Enalapril)
Innovace 5 mg, 20 mg comprimidos
¿Por qué se usa Innovace? ¿Para qué sirve?
Innovace contiene un principio activo llamado maleato de enalapril. Este principio activo pertenece a un grupo de medicamentos denominados inhibidores de la ECA (inhibidores de la enzima convertidora de angiotensina).
Se utiliza Innovace:
- para tratar la presión arterial alta (hipertensión)
- para tratar la insuficiencia cardíaca (debilitamiento de la función cardíaca). Puede reducir la necesidad de ir al hospital y puede ayudar a algunos pacientes a vivir más tiempo.
- para prevenir los signos de insuficiencia cardíaca, que incluyen: dificultad para respirar, cansancio después de una actividad física ligera como caminar o hinchazón de los tobillos y los pies.
Este medicamento actúa dilatando los vasos sanguíneos. Esto reduce su presión arterial. Por lo general, el medicamento comienza a actuar en una hora y el efecto dura al menos 24 horas. Algunas personas necesitarán varias semanas de tratamiento antes de que se pueda observar el mejor efecto sobre la presión arterial.
Contraindicaciones Cuándo no se debe utilizar Innovace
No tome Innovace
- si es alérgico al maleato de enalapril oa cualquiera de los demás componentes de este medicamento
- si ha tenido anteriormente una reacción alérgica a un tipo de medicamento similar a este medicamento llamado inhibidor de la ECA
- si ha tenido previamente hinchazón de la cara, labios, boca, lengua o garganta que le haya causado dificultad para tragar y respirar (angioedema) de naturaleza desconocida o hereditaria
- si tiene diabetes o insuficiencia renal y está siendo tratado con un medicamento para bajar la presión arterial que contiene aliskiren
- si está embarazada de más de 3 meses (también es preferible evitar el uso de Innovace al principio del embarazo; consulte la sección de embarazo).
No tome este medicamento si tiene alguno de los problemas anteriores. Si no está seguro, consulte a su médico o farmacéutico antes de tomar este medicamento.
Precauciones de uso Lo que necesita saber antes de tomar Innovace
Consulte a su médico o farmacéutico antes de tomar Innovace:
- si tiene un problema de corazón - si tiene una enfermedad que afecta a los vasos sanguíneos del cerebro
- si tiene un problema sanguíneo como bajo o falta de glóbulos blancos (neutropenia / agranulocitosis), recuentos bajos de plaquetas (trombocitopenia) o recuentos bajos de glóbulos rojos (anemia)
- si tiene un problema de hígado
- si tiene un problema de riñón (incluido un trasplante de riñón). Esto puede provocar un aumento del potasio en sangre que puede ser grave. Es posible que su médico deba ajustar la dosis de Innovace o controlar sus niveles de potasio en sangre.
- si está en diálisis
- si ha tenido vómitos excesivos o diarrea intensa recientemente
- si está siguiendo una dieta baja en sal, tomando suplementos de potasio, agentes ahorradores de potasio o sustitutos de la sal que contengan potasio
- si tiene más de 70 años
- si tiene diabetes. Es necesario controlar cuidadosamente la disminución de los niveles de glucosa en sangre, especialmente durante el primer mes de tratamiento. El nivel de potasio en sangre también puede ser más alto.
- si alguna vez ha tenido una reacción alérgica con hinchazón de la cara, labios, lengua o garganta con dificultad para tragar o respirar. Debe saber que los pacientes de raza negra tienen un mayor riesgo de sufrir este tipo de reacciones a los inhibidores de la ECA.
- si tiene la tensión arterial baja (lo nota cuando se siente débil o mareado, especialmente al ponerse de pie)
- si tiene una enfermedad vascular del colágeno (por ejemplo, lupus eritematoso, artritis reumatoide o esclerodermia), está recibiendo un tratamiento que inhibe el sistema inmunológico, está tomando los medicamentos alopurinol o procainamida o combinaciones de los mismos.
- si está tomando alguno de los siguientes medicamentos utilizados para tratar la presión arterial alta:
- un antagonista del receptor de angiotensina II (ARAII) (también conocido como sartán, por ejemplo, valsartán, telmisartán, irbesartán, etc.), especialmente si tiene problemas renales relacionados con la diabetes
- aliskiren.
Su médico puede controlar su función renal, presión arterial y la cantidad de electrolitos (por ejemplo, potasio) en su sangre a intervalos regulares Ver también la información bajo el encabezado "No tome Innovace".
Debe informar a su médico si cree que está embarazada (o si existe la posibilidad de quedarse embarazada). Este medicamento no se recomienda al principio del embarazo y no debe tomarse si está embarazada de más de 3 meses, ya que puede causar daños graves a su bebé si se usa en esta etapa (ver sección de embarazo).
Debe tener en cuenta que este medicamento reduce la presión arterial de forma menos eficaz en pacientes de raza negra que en pacientes que no son de raza negra.
Si no está seguro de si se encuentra en alguna de las situaciones anteriores, consulte a su médico o farmacéutico antes de tomar este medicamento.
Si está a punto de someterse a un procedimiento
Si está a punto de someterse a alguno de los siguientes procedimientos, informe a su médico que está tomando Innovace:
- cualquier tipo de cirugía o anestesia (incluso en el dentista)
- tratamiento que elimina el colesterol de la sangre llamado "aféresis de LDL"
- tratamiento de desensibilización para reducir los efectos de una alergia a las picaduras de abejas o avispas.
Si se encuentra en alguna de las situaciones anteriores, hable con su médico o dentista antes del procedimiento.
Interacciones ¿Qué medicamentos o alimentos pueden cambiar el efecto de Innovace?
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o podría tener que tomar cualquier otro medicamento. Se incluyen las medicinas a base de hierbas. Esto se debe a que Innovace puede interferir con la forma en que actúan algunos medicamentos. Algunos otros medicamentos también pueden interferir con la forma en que actúa Innovace. Su médico puede necesitar cambiar su dosis y / o tomar otras precauciones.
En particular, informe a su médico o farmacéutico si está tomando alguno de los siguientes medicamentos:
- un antagonista del receptor de angiotensina II (AIIRA) o aliskiren (ver también la información bajo "No tome Innovace" y "Advertencias y precauciones"
- otros medicamentos para bajar la presión arterial, como betabloqueantes o diuréticos - medicamentos que contienen potasio (incluidos los sucedáneos de la sal en la dieta)
- medicamentos para la diabetes (incluidos antidiabéticos orales e insulina)
- litio (un medicamento utilizado para tratar cierto tipo de depresión)
- medicamentos para la depresión llamados "antidepresivos tricíclicos" - medicamentos para problemas mentales llamados "antipsicóticos"
- algunos medicamentos para la tos y el resfriado y medicamentos que reducen el peso corporal que contienen el llamado "agente simpaticomimético"
- algunos medicamentos para el dolor o la artritis, incluida la terapia con sales de oro; medicamentos antiinflamatorios no esteroideos, incluidos los inhibidores de la COX-2 (medicamentos que reducen la inflamación y que pueden usarse para ayudar a aliviar el dolor)
- aspirina (ácido acetilsalicílico)
- medicamentos utilizados para disolver los coágulos de sangre (trombolíticos) - alcohol
Si no está seguro de si algo de lo anterior le aplica, hable con su médico o farmacéutico antes de tomar Innovace.
Innovace con alimentos y bebidas
Innovace se puede tomar con o sin alimentos. La mayoría de las personas toman Innovace con un vaso de agua.
Advertencias Es importante saber que:
Embarazo y lactancia
El embarazo
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico antes de utilizar este medicamento. Por lo general, su médico le recomendará que deje de tomar Innovace antes de quedarse embarazada o tan pronto como sepa que está embarazada y le recomendará que tome otro medicamento en lugar de Innovace. Este medicamento no se recomienda para todos los "embarazos precoces y no debe tomarse si está embarazada de más de tres meses, ya que puede causar daños graves a su bebé si se toma después del tercer mes de embarazo.
Hora de la comida
Informe a su médico si está amamantando o si necesita comenzar a amamantar. No se recomienda amamantar a los bebés (primeras semanas después del nacimiento), especialmente a los bebés prematuros, mientras usa este medicamento. En el caso de niños mayores, su médico le informará de los riesgos y beneficios de tomar este medicamento durante la lactancia, en comparación con otros tratamientos.
Conducción y uso de máquinas
Puede experimentar mareos o somnolencia mientras toma este medicamento. Si esto sucede, no conduzca ni utilice herramientas o maquinaria.
Innovace contiene lactosa
Innovace contiene lactosa, que es un tipo de azúcar. Si su médico le ha indicado que padece una intolerancia a ciertos azúcares, consulte con él antes de tomar este medicamento.
Dosis, método y momento de administración Cómo utilizar Innovace: Posología
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte a su médico o farmacéutico.
- Es muy importante seguir tomando este medicamento durante el tiempo que su médico se lo recete.
- No tome más comprimidos de los recetados.
Alta presión sanguínea
- La dosis inicial habitual varía de 5 a 20 mg una vez al día.
- Algunos pacientes pueden necesitar comenzar el tratamiento con una dosis más baja.
- La dosis de mantenimiento habitual es de 20 mg una vez al día.
- La dosis máxima de mantenimiento es de 40 mg una vez al día.
Insuficiencia cardiaca
- La dosis inicial habitual es de 2,5 mg una vez al día.
- Su médico aumentará gradualmente la dosis hasta alcanzar la dosis adecuada para usted.
- La dosis de mantenimiento habitual es de 20 mg al día, administrada en una o dos dosis.
- La dosis máxima de mantenimiento es de 40 mg al día, dividida en dos administraciones.
Pacientes con problemas renales
La dosis del medicamento variará según el funcionamiento de sus riñones:
- problemas renales moderados - 5 a 10 mg por día
- problemas renales graves: 2,5 mg al día
- si está en diálisis - 2,5 mg por día. En los días en que no esté en diálisis, la dosis puede variar de acuerdo con su presión arterial.
Pacientes de edad avanzada
La dosis la decidirá su médico y se basará en el funcionamiento de sus riñones.
Uso en niños
La experiencia con el uso de Innovace en niños con presión arterial alta es limitada. Si el niño puede tragar los comprimidos, la dosis se basará en el peso y la presión arterial del niño. Las dosis iniciales habituales son:
- peso entre 20 kg y 50 kg - 2,5 mg por día
- peso superior a 50 kg - 5 mg por día.
La dosis se puede cambiar según las necesidades del niño:
- Se puede utilizar una dosis máxima de 20 mg al día en niños que pesen entre 20 kg y 50 kg.
- Se puede utilizar una dosis máxima de 40 mg al día en niños que pesen más de 50 kg.
Este medicamento no se recomienda en bebés (primeras semanas de vida) y niños con problemas renales.
Sobredosis Qué hacer si ha tomado demasiado Innovace
Si toma más Innovace del que debiera
Si toma más Innovace del que debiera, informe a su médico o acuda a un hospital de inmediato. Lleve el paquete de medicamentos con usted. Pueden producirse los siguientes efectos: aturdimiento o mareos. Esto se debe a una caída repentina o excesiva de la presión arterial.
Si olvidó tomar Innovace
- Si olvidó tomar una tableta, omita la dosis olvidada.
- Tome la siguiente dosis como de costumbre.
- No tome una dosis doble para compensar las dosis olvidadas.
Si deja de tomar Innovace
No deje de tomar el medicamento a menos que su médico se lo indique. Si tiene más preguntas sobre el uso de este medicamento, consulte a su médico o farmacéutico.
Efectos secundarios ¿Cuáles son los efectos secundarios de Innovace?
Como todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Los siguientes efectos secundarios pueden ocurrir con este medicamento:
Deje de tomar Innovace y póngase en contacto con un médico de inmediato si nota alguno de los siguientes síntomas:
- hinchazón de la cara, labios, lengua o garganta que puede causar dificultad para respirar o tragar
- hinchazón de manos, pies o tobillos
- desarrollo de una erupción con protuberancias rojas elevadas (urticaria).
Debe tener en cuenta que los pacientes de raza negra tienen un mayor riesgo de desarrollar este tipo de reacción. Si nota alguno de estos síntomas, deje de tomar Innovace y póngase en contacto con su médico de inmediato.
Puede sentirse débil o mareado cuando comience a tomar este medicamento. Si esto sucede, puede ser útil recostarse. Esto es causado por la presión arterial baja. Debería mejorar a medida que continúe tomando el medicamento. Si está preocupado, comuníquese con su médico.
Otros efectos secundarios incluyen:
Muy frecuentes (pueden afectar a más de 1 de cada 10 personas)
- sensación de mareo, debilidad o malestar
- visión borrosa
- tos
Frecuentes (pueden afectar hasta 1 de cada 10 personas)
- confusión mental debido a la presión arterial baja, cambios en el ritmo cardíaco, latidos cardíacos rápidos, angina de pecho o dolor en el pecho
- dolor de cabeza, depresión, desmayo (síncope)
- sentido del gusto alterado
- dificultad para respirar
- diarrea, dolor abdominal
- cansancio (fatiga)
- erupción, reacciones alérgicas con hinchazón de la cara, labios, lengua o garganta con dificultad para respirar o tragar
- niveles elevados de potasio en sangre, niveles elevados de creatinina en sangre (ambos suelen encontrarse en una prueba de laboratorio
Poco frecuentes (pueden afectar hasta 1 de cada 100 personas)
- enrojecimiento
- caída repentina de la presión arterial
- latidos cardíacos rápidos o irregulares (palpitaciones)
- ataque cardíaco (posiblemente debido a una presión arterial muy baja en algunos pacientes de alto riesgo, incluidos aquellos con problemas circulatorios en el corazón o el cerebro)
- accidente cerebrovascular (posiblemente debido a una presión arterial muy baja en pacientes de alto riesgo)
- anemia (incluida anemia aplásica y hemolítica)
- confusión, insomnio o somnolencia, nerviosismo
- sensación de hormigueo o entumecimiento en la piel
- vértigo (sensación de mareo)
- zumbido en los oídos (tinnitus)
- secreción nasal, dolor de garganta o ronquera: asma asociada con opresión en el pecho
- tránsito lento de alimentos en el intestino (íleo), inflamación del páncreas
- malestar (vómitos), dificultad para digerir, estreñimiento, pérdida del apetito
- malestar estomacal (irritación gástrica), sequedad de boca, úlcera
- calambres musculares
- función renal alterada, insuficiencia renal
- aumento de la sudoración
- picazón o urticaria
- perdida de cabello
- sensación general de malestar, temperatura corporal alta (fiebre)
- impotencia
- alto nivel de proteína en la orina (medido en una prueba de laboratorio)
- niveles bajos de azúcar o sodio en sangre, niveles altos de urea en sangre (todos medidos en un análisis de sangre)
Raras (pueden afectar hasta 1 de cada 1.000 personas)
- "Fenómeno de Raynaud" en el que las manos y los pies pueden volverse muy fríos y blancos debido a un flujo sanguíneo bajo
- cambios en los valores sanguíneos, como disminución del número de glóbulos blancos y rojos, disminución de la hemoglobina, disminución del número de plaquetas
- depresión de la médula ósea
- hinchazón de las glándulas del cuello, las axilas o la ingle
- Enfermedades autoinmunes
- sueños extraños o alteraciones del sueño
- acumulación de líquido u otras sustancias en los pulmones (evidenciada por rayos X)
- inflamación de la nariz
- inflamación de los pulmones que causa dificultad para respirar (neumonía)
- inflamación de las mejillas, encías, lengua, labios, garganta
- disminución de la cantidad de orina
- erupción en forma de diana (eritema multiforme)
- "Síndrome de Stevens-Johnson" y "necrólisis epidérmica tóxica" (afecciones cutáneas graves en las que hay enrojecimiento y descamación de la piel, úlceras ampollosas o expuestas), dermatitis exfoliativa / eritrodermia (erupción grave con descamación o descamación de la capa superficial de la piel), pénfigo ( pequeñas ampollas llenas de líquido en la piel)
- problemas del hígado o de la vesícula biliar como disminución de la función hepática, inflamación del hígado, ictericia (coloración amarillenta de la piel o los ojos), niveles altos de enzimas hepáticas o bilirrubina (medida en un análisis de sangre)
- agrandamiento de las mamas en los hombres (ginecomastia)
Muy raros (pueden afectar hasta 1 de cada 10.000 personas)
- hinchazón en los intestinos (angioedema intestinal)
Frecuencia no conocida (la frecuencia no puede estimarse a partir de los datos disponibles)
- sobreproducción de hormona antidiurética, que causa retención de líquidos, lo que resulta en debilidad, cansancio o confusión
- Se ha informado de un complejo de síntomas que puede incluir algunos o todos los siguientes: fiebre, inflamación de los vasos sanguíneos (serositis / vasculitis), dolor muscular (mialgia / miositis), dolor articular (artralgia / artritis). Puede producirse erupción cutánea, fotosensibilidad u otras manifestaciones cutáneas.
Notificación de efectos secundarios
Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluidos los posibles efectos adversos que no aparecen en este prospecto. También puede notificar efectos secundarios directamente a través del sistema nacional de notificación en: https://www.aifa.gov.it/content/segnalazioni-reazioni-avversei Al notificar efectos secundarios, puede ayudar a proporcionar más información sobre la seguridad de este medicamento.
Caducidad y retención
Mantenga este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en el blister y la caja después de CAD. La fecha de caducidad se refiere al último día de ese mes.
No conservar por encima de 25 ° C.
Conservar en el envase original para protegerlo de la humedad No tirar ningún medicamento por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. Esto ayudará a proteger el medio ambiente.
Qué contiene Innovace
- El ingrediente activo es el maleato de enalapril (5 mg o 20 mg).
- Los demás componentes son lactosa monohidrato, hidrogenocarbonato de sodio, almidón de maíz, almidón de maíz pregelatinizado, estearato de magnesio. Los comprimidos de 20 mg también contienen óxido de hierro rojo (E172) y óxido de hierro amarillo (E172).
Aspecto de Innovace y contenido del envase
Innovace está disponible en los siguientes tamaños de envase:
ENAPREN 5 mg en blísters de aluminio que contienen 2, 14, 20, 28, 28 x 1, 30, 49 x 1, 50, 60, 98 o 100 comprimidos.
ENAPREN 20 mg en blísteres de aluminio que contienen 10, 14, 20, 28, 28 x 1, 30, 49 x 1, 50, 56, 60, 84, 90, 98, 100 o 500 comprimidos. Es posible que no se comercialicen todos los tamaños de envases.
Prospecto fuente: AIFA (Agencia Italiana de Medicamentos). Contenido publicado en enero de 2016. Es posible que la información presente no esté actualizada.
Para tener acceso a la versión más actualizada, es recomendable acceder al sitio web de la AIFA (Agencia Italiana de Medicamentos). Descargo de responsabilidad e información útil.
01.0 NOMBRE DEL MEDICAMENTO
TABLETAS ENAPREN
02.0 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Innovace 5 mg.
Cada comprimido contiene 5 mg de maleato de enalapril.
Excipiente: cada comprimido contiene 196 mg de lactosa monohidrato.
Innovace 20 mg.
Cada comprimido contiene 20 mg de maleato de enalapril.
Excipiente: cada comprimido contiene 147 mg de lactosa monohidrato.
Excipiente (s) con efectos conocidos:
Para consultar la lista completa de excipientes, ver sección 6.1.
03.0 FORMA FARMACÉUTICA
Tableta.
5 mg
blanco, de forma redonda, con marca de fractura en un lado * e impreso con 712 en el otro.
20 magnesio
color melocotón, de forma redonda, con un cuarto de fractura en un lado * e impreso con 714 en el otro.
* La marca de fractura solo tiene como objetivo facilitar la rotura para facilitar la administración oral y no tiene como objetivo dividir el comprimido en dosis iguales.
04.0 INFORMACIÓN CLÍNICA
04.1 Indicaciones terapéuticas
• Tratamiento de la hipertensión.
• Tratamiento de insuficiencia cardíaca sintomática.
• Prevención de la insuficiencia cardíaca sintomática en pacientes con disfunción ventricular izquierda asintomática (fracción de eyección ≤35%).
(Ver sección 5.1)
04.2 Posología y forma de administración
Dosis
Los alimentos no interfieren con la absorción de los comprimidos de Innovace.
La dosis debe adaptarse al perfil del paciente (ver sección 4.4) y a la respuesta de la presión arterial.
Población pediátrica
La experiencia con el uso de Innovace en ensayos clínicos en pacientes pediátricos hipertensos es limitada (ver secciones 4.4, 5.1 y 5.2).
Hipertensión
La dosis inicial es de 5 mg hasta un máximo de 20 mg, según el grado de hipertensión y el estado del paciente (ver más abajo). Innovace se administra una vez al día. Para la hipertensión leve, la dosis inicial recomendada es de 5 a 10 mg. Los pacientes con un sistema renina-angiotensina-aldosterona intensamente activado (por ejemplo, aquellos con hipertensión renovascular, depleción de sal y / o hipovolemia, descompensación o hipertensión severa) pueden experimentar una caída excesiva en presión arterial después de la dosis inicial Se recomienda una dosis inicial de 5 mg o menos en estos pacientes y el inicio del tratamiento debe realizarse bajo estrecha supervisión médica.
El tratamiento previo con diuréticos a altas dosis puede producir hipovolemia y riesgo de hipotensión al iniciar el tratamiento con enalapril. En estos pacientes se recomienda una dosis inicial de 5 mg o menos. Si es posible, se debe interrumpir el tratamiento con diuréticos durante 2-3 días antes de iniciar el tratamiento con Innovace. Se debe controlar la función renal y el potasio sérico.
La dosis de mantenimiento habitual es de 20 mg / día. La dosis máxima de mantenimiento es de 40 mg / día.
Insuficiencia cardíaca / disfunción ventricular izquierda asintomática
En el tratamiento de la insuficiencia cardíaca sintomática, Innovace se utiliza junto con diuréticos y, en su caso, digitálicos o betabloqueantes. La dosis inicial de Innovace en pacientes con insuficiencia cardíaca sintomática o disfunción ventricular izquierda asintomática es de 2,5 mg y debe administrarse bajo estrecha observación médica para determinar el efecto inicial sobre la presión arterial. En ausencia de hipotensión sintomática posterior al brote. Inicio del tratamiento con Innovace para la insuficiencia cardíaca, o después de un tratamiento exitoso del mismo, la dosis debe aumentarse gradualmente, en función de la tolerabilidad del paciente, hasta la dosis de mantenimiento habitual de 20 mg, administrada como dosis única o dividida en 2 dosis. un período de 2-4 semanas La dosis máxima es de 40 mg administrados en dos dosis divididas.
Tabla 1: Titulación de la dosis sugerida de Innovace
en pacientes con insuficiencia cardíaca / disfunción ventricular izquierda asintomática
* Se deben tomar las precauciones adecuadas en pacientes que reciben diuréticos y aquellos con insuficiencia renal (ver sección 4.4).
La presión arterial y la función renal deben controlarse estrechamente antes y después del inicio del tratamiento con Innovace (ver sección 4.4) ya que se han notificado casos de hipotensión y (más raramente) insuficiencia renal posterior. En pacientes tratados con diuréticos, la dosis debe reducirse si es posible. antes de iniciar el tratamiento con Innovace.La aparición de hipotensión después de la dosis inicial de Innovace no implica que la hipotensión vuelva durante el tratamiento crónico con Innovace y no impide el uso continuado del medicamento.También se deben controlar el potasio sérico y la función renal.
Posología en insuficiencia renal
En general, los intervalos entre las dosis de enalapril deben prolongarse y / o reducirse la dosis.
Tabla 2: Posología en insuficiencia renal
* ver sección 4.4. Enalaprilato es dializable, la dosis en los días en que los pacientes no están en diálisis debe ajustarse de acuerdo con la respuesta de la presión arterial.
Uso en ancianos
La dosis debe estar en consonancia con la función renal del paciente de edad avanzada (ver sección 4.4).
Uso pediátrico
Para los pacientes que pueden tragar comprimidos, la dosis debe ajustarse de acuerdo con el perfil del paciente y la respuesta de la presión arterial. La dosis inicial recomendada es de 2,5 mg en pacientes de 20 a
No se recomienda Innovace en neonatos y pacientes pediátricos con tasa de filtración glomerular 2 ya que no hay datos disponibles.
Método de administración
Uso oral.
04.3 Contraindicaciones
• Hipersensibilidad al principio activo oa alguno de los excipientes incluidos en la sección 6.1 oa otros inhibidores de la ECA.
• Antecedentes de angioedema asociado con la terapia con inhibidores de la ECA.
• Angioedema hereditario o idiopático.
• Segundo y tercer trimestre del embarazo (ver secciones 4.4 y 4.6).
• El uso concomitante de Innovace con productos que contienen aliskiren está contraindicado en pacientes con diabetes mellitus o insuficiencia renal (TFG 2) (ver secciones 4.5 y 5.1).
04.4 Advertencias especiales y precauciones de uso apropiadas
Hipotensión sintomática
Rara vez se ha informado hipotensión sintomática en pacientes con hipertensión no complicada. En pacientes hipertensos que reciben Innovace, es más probable que se produzca hipotensión sintomática si el paciente es hipovolémico, por ejemplo, aquellos tratados con diuréticos, pacientes con una dieta baja en sodio, pacientes en hemodiálisis, pacientes con diarrea o vómitos (ver secciones 4.5 y 4.8). Se ha observado hipotensión sintomática en pacientes con insuficiencia cardíaca, con o sin insuficiencia renal asociada. Esto es más probable que ocurra en aquellos pacientes con grados más graves de insuficiencia cardíaca, como se refleja en el uso de dosis altas. Diuréticos de asa, hiponatremia o alteraciones función renal. En estos pacientes, el tratamiento debe iniciarse bajo supervisión médica y se debe seguir de cerca a los pacientes siempre que se ajuste la dosis de Innovace y / o el diurético.
Se pueden aplicar consideraciones similares a pacientes con cardiopatía isquémica o con una "enfermedad cerebrovascular, en la que una caída excesiva de la presión arterial podría provocar un infarto de miocardio o un accidente cerebrovascular".
Si se produce hipotensión, se debe colocar al paciente en decúbito supino y, si es necesario, se le debe administrar una infusión de solución salina intravenosa. Una respuesta hipotensiva transitoria no es una contraindicación para dosis adicionales, que generalmente se pueden administrar sin dificultad una vez que la presión arterial ha aumentado después del aumento de volumen.
El tratamiento con Innovace puede provocar una disminución adicional de la presión arterial en algunos pacientes con insuficiencia cardíaca con presión arterial normal o baja. Este efecto es de esperar y generalmente no es necesario suspender el tratamiento. Si la hipotensión se vuelve sintomática, es necesario reducir la dosis y / o suspender el diurético y / o Innovace.
Estenosis de la válvula aórtica o mitral / miocardiopatía hipertrófica
Como todos los vasodilatadores, los inhibidores de la ECA deben usarse con precaución en pacientes con obstrucción del tracto de salida del ventrículo izquierdo y valvular y deben evitarse en caso de shock cardiogénico y obstrucción hemodinámica significativa.
Insuficiencia renal
En caso de insuficiencia renal (aclaramiento de creatinina
Se ha notificado insuficiencia renal asociada a enalapril y se ha producido principalmente en pacientes con insuficiencia cardíaca grave y enfermedad renal subyacente, incluida la estenosis de la arteria renal. Si se reconoce temprano y se trata adecuadamente, la insuficiencia renal asociada al tratamiento con enalapril suele ser reversible.
Algunos pacientes hipertensos sin enfermedad renal preexistente aparente han desarrollado aumentos en la urea y creatinina en sangre cuando se administró enalapril concomitantemente con un diurético. Puede ser necesario reducir la dosis de enalapril y / o suspender el diurético. Esta circunstancia debe poner en duda la posibilidad de una estenosis de la arteria renal básica (ver sección 4.4.Hipertensión renovascular).
Hipertensión renovascular
En pacientes con estenosis bilateral de la arteria renal o estenosis de la arteria del único riñón funcional tratado con inhibidores de la ECA, existe un mayor riesgo de hipotensión e insuficiencia renal. La pérdida de la función renal puede ocurrir incluso con cambios leves en la creatinina sérica. En estos pacientes, el tratamiento debe iniciarse bajo estrecha supervisión médica con dosis bajas, titulación cuidadosa y control de la función renal.
Transplante de riñón
No hay experiencia clínica con la administración de Innovace en pacientes con un trasplante de riñón reciente. Por tanto, no se recomienda el tratamiento con Innovace.
Insuficiencia hepática
En raras ocasiones, los inhibidores de la ECA se han asociado con un síndrome que comienza con ictericia colestásica o hepatitis y progresa a necrosis hepática fulminante y (a veces) a la muerte. Se desconoce el mecanismo de este síndrome. Los pacientes que toman inhibidores de la ECA y desarrollan ictericia o elevaciones marcadas de las enzimas hepáticas deben suspender el inhibidor de la ECA y someterse a un seguimiento médico adecuado.
Neutropenia / agranulocitosis
Se han notificado casos de neutropenia / agranulocitosis, trombocitopenia y anemia en pacientes tratados con inhibidores de la ECA. En pacientes con función renal normal y sin complicaciones, la neutropenia ocurre raramente. Enalapril debe usarse con extrema precaución en pacientes con enfermedad del colágeno vascular, terapia inmunosupresora, tratamientos con alopurinol o procainamida o una combinación de estas complicaciones, especialmente si existe insuficiencia renal preexistente. Algunos de estos pacientes han desarrollado infecciones graves que en algunos casos no han respondido a la terapia intensiva con antibióticos. Cuando se usa enalapril en estos pacientes, se recomienda un control periódico de los leucocitos y se debe indicar a los pacientes que notifiquen cualquier signo de infección.
Hipersensibilidad / edema angioneurótico
Se ha notificado edema angioneurótico de la cara, extremidades, labios, lengua, glotis y / o laringe en pacientes tratados con inhibidores de la enzima convertidora de angiotensina, incluido Enapren. Esto puede ocurrir en cualquier momento durante el tratamiento. En tales casos, Innovace debe suspenderse de inmediato e instituirse un control adecuado para garantizar la regresión completa de los síntomas antes de que el paciente sea dado de alta. Incluso en los casos en los que el edema se limita solo a la lengua, sin dificultad respiratoria, los pacientes pueden requerir una observación prolongada, ya que el tratamiento con antihistamínicos y cortisonas puede no ser suficiente.
En muy raras ocasiones, se han notificado muertes por angioedema asociado con edema laríngeo o edema lingual. Es probable que se produzca obstrucción de las vías respiratorias en pacientes con afectación de la lengua, la glotis o la laringe, especialmente si tienen antecedentes positivos de cirugía de las vías respiratorias. debe administrarse con prontitud y / o mantenerse una vía aérea permeable.
Se ha informado que los pacientes de raza negra que reciben inhibidores de la ECA tienen una mayor incidencia de angioedema que los pacientes que no son de raza negra.
Los pacientes con antecedentes de angioedema no relacionado con el tratamiento con inhibidores de la ECA pueden tener un mayor riesgo de angioedema durante el tratamiento con un inhibidor de la ECA (ver también sección 4.3).
Reacciones anafilactoides durante la desensibilización a himenópteros
En raras ocasiones, los pacientes en tratamiento con inhibidores de la ECA han informado reacciones anafilactoides potencialmente mortales durante la desensibilización con veneno de himenópteros. Estas reacciones se evitaron suspendiendo temporalmente la terapia con inhibidores de la ECA antes de cada desensibilización.
Reacciones anafilactoides en el curso de la aféresis de LDL
En raras ocasiones, algunos pacientes en tratamiento con inhibidores de la ECA que se sometieron a aféresis de lipoproteínas de baja densidad (LDL) con sulfato de dextrano han desarrollado reacciones anafilactoides potencialmente mortales. Estas reacciones se evitaron interrumpiendo temporalmente la terapia con inhibidores de la ECA antes de cada sesión de aféresis.
Pacientes en hemodiálisis
Se han notificado reacciones anafilactoides en pacientes dializados con membranas de alto flujo (p. Ej. AN 69) y tratados al mismo tiempo con un inhibidor de la ECA. Para tales pacientes, se debe considerar el uso de un tipo diferente de membrana de diálisis o una clase diferente de agentes antihipertensivos.
Hipoglucemia
Se debe aconsejar a los pacientes diabéticos tratados con antidiabéticos orales o insulina que inicien el tratamiento con un inhibidor de la ECA que vigilen estrechamente la aparición de hipoglucemia, especialmente durante el primer mes de uso concomitante (ver sección 4.5).
Tos
Se ha informado tos con el uso de inhibidores de la ECA. La tos es típicamente no productiva, persistente y se resuelve al suspender el tratamiento. La tos inducida por inhibidores de la ECA debe considerarse en el diagnóstico diferencial de la tos.
Cirugía / Anestesia
En pacientes sometidos a cirugía mayor o durante la anestesia con agentes que provocan hipotensión, el enalapril bloquea la formación de angiotensina II secundaria a la liberación compensadora de renina, la hipotensión que se produce en estos casos puede corregirse mediante un aumento del volumen sanguíneo.
Hiperpotasemia
Se han observado elevaciones del potasio sérico en algunos pacientes tratados con inhibidores de la ECA, incluido enalapril. Los factores de riesgo para el desarrollo de hiperpotasemia incluyen insuficiencia renal, empeoramiento de la función renal, edad (> 70 años), diabetes mellitus, eventos ocurridos, particularmente deshidratación, insuficiencia cardíaca aguda, acidosis metabólica y uso concomitante de diuréticos. Ahorro de potasio (p. Ej., Espironolactona , eplerenona, triamtereno o amilorida), suplementos de potasio o sustitutos de la sal que contienen potasio; o el uso concomitante de otros fármacos asociados con aumentos del potasio sérico (p. ej., heparina). Particularmente en pacientes con insuficiencia renal, el uso de diuréticos ahorradores de potasio, suplementos de potasio o sustitutos de la sal que contienen potasio puede conducir a un aumento significativo del potasio sérico. . La hiperpotasemia puede causar arritmias graves, a veces mortales. Si se considera apropiado el uso concomitante de enalapril y cualquiera de los medicamentos anteriores, deben usarse con precaución y con un control frecuente del potasio sérico (ver sección 4.5).
Litio
En general, no se recomienda la combinación de litio y enalapril (ver sección 4.5).
Doble bloqueo del sistema renina-angiotensina-aldosterona (RAAS)
Existe evidencia de que el uso concomitante de inhibidores de la ECA, bloqueantes de los receptores de angiotensina II o aliskiren aumenta el riesgo de hipotensión, hiperpotasemia y disminución de la función renal (incluida la insuficiencia renal aguda). Por tanto, no se recomienda el bloqueo doble del SRAA mediante el uso combinado de inhibidores de la ECA, bloqueantes de los receptores de angiotensina II o aliskiren (ver secciones 4.5 y 5.1).
Si la terapia de doble bloqueo se considera absolutamente necesaria, solo debe realizarse bajo la supervisión de un especialista y con un control estrecho y frecuente de la función renal, los electrolitos y la presión arterial.
Los inhibidores de la ECA y los antagonistas de los receptores de angiotensina II no deben usarse concomitantemente en pacientes con nefropatía diabética.
Lactosa
Innovace contiene lactosa y, por tanto, los pacientes con problemas hereditarios raros de intolerancia a la galactosa, deficiencia de lactasa o malabsorción de glucosa o galactosa no deben tomar este medicamento.
Innovace contiene menos de 200 mg de lactosa por comprimido.
Población pediátrica
Existe experiencia limitada en términos de eficacia y seguridad en niños hipertensos mayores de 6 años, pero no hay experiencia para las otras indicaciones. Se dispone de datos farmacocinéticos limitados en niños mayores de 2 meses (ver también las secciones 4.2, 5.1 y 5.2). No se recomienda Innovace en niños para otras indicaciones distintas de la hipertensión.
No se recomienda Innovace en neonatos y pacientes pediátricos con tasa de filtración glomerular.
El embarazo
La terapia con inhibidores de la ECA no debe iniciarse durante el embarazo. A menos que se considere esencial continuar el tratamiento con inhibidores de la ECA, las pacientes que estén planeando quedarse embarazadas deben cambiar a un tratamiento antihipertensivo alternativo que tenga un perfil de seguridad establecido para su uso durante el embarazo. necesario, se debe iniciar un tratamiento alternativo (ver secciones 4.3 y 4.6).
Diferencias étnicas
Al igual que con otros inhibidores de la enzima convertidora de angiotensina, enalapril parece ser menos eficaz para reducir la presión arterial en personas de raza negra que en personas de otra raza, posiblemente debido a una alta prevalencia de niveles bajos de renina en la sangre.
04.5 Interacciones con otros medicamentos y otras formas de interacción
Doble bloqueo del sistema renina-angiotensina-aldosterona (RAAS)
Los datos de ensayos clínicos han demostrado que el bloqueo dual del sistema renina-angiotensina-aldosterona (SRAA) mediante el uso combinado de inhibidores de la ECA, bloqueadores del receptor de angiotensina II o aliskiren se asocia con una mayor frecuencia de reacciones adversas, como hipotensión, hiperpotasemia y disminución función renal (incluida la insuficiencia renal aguda) en comparación con el uso de un único agente activo en el sistema RAAS (ver secciones 4.3, 4.4 y 5.1).
Diuréticos ahorradores de potasio y suplementos de potasio
Los inhibidores de la ECA reducen la pérdida de potasio inducida por diuréticos. Los diuréticos ahorradores de potasio (p. Ej., Espironolactona, eplerenona, triamtereno y amilorida), los suplementos de potasio o los sustitutos de la sal que contienen potasio pueden producir aumentos significativos del potasio sérico. Si está indicado el uso concomitante debido a una hipopotasemia demostrada, deben usarse con precaución y con un control frecuente del potasio sérico (ver sección 4.4).
Diuréticos (tiazidas o diuréticos de asa)
El tratamiento previo con diuréticos a altas dosis puede provocar una depleción de volumen y un riesgo de hipotensión al iniciar el tratamiento con enalapril (ver sección 4.4). Los efectos hipotensores pueden reducirse interrumpiendo los diuréticos, aumentando el volumen sanguíneo o tomando sales o iniciando el tratamiento con una dosis baja de enalapril.
Otros agentes antihipertensivos
El uso concomitante de estos medicamentos puede aumentar el efecto hipotensor de enalapril. El uso concomitante con nitroglicerina y otros nitratos u otros vasodilatadores puede reducir aún más la presión arterial.
Litio
Se han notificado aumentos reversibles de las concentraciones séricas de litio y episodios de toxicidad por litio durante la administración concomitante de litio e inhibidores de la ECA. El uso concomitante de diuréticos tiazídicos puede aumentar aún más los niveles de litio y aumentar el riesgo de toxicidad por litio con inhibidores de la ECA. No se recomienda el uso de enalapril con litio, pero si la combinación es necesaria, se debe vigilar cuidadosamente los niveles séricos de litio (ver sección 4.4).
Antidepresivos tricíclicos / Antipsicóticos / Anestésicos / Narcóticos
El uso concomitante de algunos medicamentos anestésicos, antidepresivos tricíclicos y antipsicóticos con inhibidores de la ECA puede producir una reducción adicional de la presión arterial (ver sección 4.4).
Medicamentos antiinflamatorios no esteroideos (AINE), incluidos los inhibidores selectivos de la ciclooxigenasa-2 (COX-2).
Los fármacos antiinflamatorios no esteroideos (AINE), incluidos los inhibidores selectivos de la ciclooxigenasa-2 (inhibidores de la COX-2), pueden reducir el efecto de los diuréticos y otros fármacos antihipertensivos. AINE, incluidos los inhibidores selectivos de la COX-2.
La administración concomitante de AINE (incluidos los inhibidores de la COX-2) y antagonistas del receptor de angiotensina II o inhibidores de la ECA tiene un efecto aditivo sobre el aumento del potasio sérico y puede provocar un deterioro de la función renal. Estos efectos suelen ser reversibles. Rara vez puede producirse insuficiencia renal aguda, especialmente en pacientes con insuficiencia renal (como los ancianos o pacientes con depleción de volumen, incluidos los que reciben tratamiento con diuréticos). Por lo tanto, la combinación debe administrarse con precaución en pacientes con insuficiencia renal Los pacientes deben estar adecuadamente hidratados y se debe considerar la monitorización de la función renal después del inicio de la terapia concomitante y posteriormente de forma periódica.
Auroterapia
Raramente se han notificado reacciones nitritoides (cuyos síntomas incluyen enrojecimiento facial, náuseas, vómitos e hipotensión) en pacientes que reciben sales de oro inyectables (aurotiomalato de sodio) con el uso concomitante de inhibidores de la ECA, incluido l "enalapril".
Simpaticomiméticos
Los simpaticomiméticos pueden reducir los efectos antihipertensivos de los inhibidores de la ECA.
Antidiabéticos
Los estudios epidemiológicos han sugerido que la administración concomitante de inhibidores de la ECA y medicamentos antidiabéticos (insulinas, hipoglucemiantes orales) puede provocar un aumento del efecto hipoglucemiante con riesgo de hipoglucemia. Este efecto parece ser más probable durante las primeras semanas de tratamiento. tratamiento combinado y en pacientes con insuficiencia renal (ver secciones 4.4 y 4.8).
Alcohol
El alcohol aumenta el efecto hipotensor de los inhibidores de la ECA.
Ácido acetilsalicílico, trombolíticos y betabloqueantes
Enalapril se puede administrar de forma segura concomitantemente con ácido acetilsalicílico (en dosis cardiológicas), trombolíticos y betabloqueantes.
Población pediátrica
Los estudios de interacciones solo se han realizado en adultos.
04.6 Embarazo y lactancia
El embarazo
Inhibidores de la ECA:
No se recomienda el uso de inhibidores de la ECA durante el primer trimestre del embarazo (ver sección 4.4) El uso de inhibidores de la ECA está contraindicado durante el segundo y tercer trimestre del embarazo (ver secciones 4.3 y 4.4).
La evidencia epidemiológica sobre el riesgo de teratogenicidad después de la exposición a inhibidores de la ECA durante el primer trimestre del embarazo no ha sido concluyente; sin embargo, no se puede excluir un pequeño aumento del riesgo. A menos que se considere esencial continuar con el tratamiento con inhibidores de la ECA, las pacientes que planean quedarse embarazadas deben cambiar a un tratamiento antihipertensivo alternativo que tenga un perfil de seguridad establecido para su uso durante el embarazo.
Cuando se diagnostica un embarazo, se debe interrumpir inmediatamente el tratamiento con inhibidores de la ECA y, si es necesario, iniciar un tratamiento alternativo.
Se sabe que la exposición al tratamiento con inhibidores de la ECA durante el segundo y tercer trimestre del embarazo induce fetotoxicidad en humanos (función renal disminuida, oligohidramnios, retraso de la osificación del cráneo) y toxicidad neonatal (insuficiencia renal, hipotensión, hiperpotasemia) (ver sección 5.3). Ha habido casos de oligohidramnios, que presumiblemente indican una disminución de la función renal fetal y que pueden causar contracturas en las extremidades, deformaciones craneofaciales y desarrollo de hipoplasia pulmonar.
En caso de que se haya producido una exposición a los inhibidores de la ECA a partir del segundo trimestre del embarazo, se recomienda un control ecográfico de la función renal y del cráneo.
Los recién nacidos cuyas madres hayan tomado inhibidores de la ECA deben ser controlados de cerca para detectar hipotensión (ver secciones 4.3 y 4.4).
Hora de la comida
Los datos farmacocinéticos limitados demuestran concentraciones muy bajas en la leche materna (ver sección 5.2). Aunque estas concentraciones parecen ser clínicamente irrelevantes, no se recomienda el uso de Innovace durante la lactancia en lactantes prematuros y en las primeras semanas después del parto debido al hipotético riesgo de efectos cardiovasculares y renales y porque no hay suficiente experiencia clínica. En el caso de bebés mayores, se puede considerar el uso de Innovace durante la lactancia si este tratamiento es necesario para la madre, pero en este caso se debe realizar un seguimiento del bebé para detectar posibles efectos adversos.
04.7 Efectos sobre la capacidad para conducir y utilizar máquinas
Al conducir o utilizar máquinas, debe tenerse en cuenta que ocasionalmente se han notificado mareos y fatiga.
04.8 Efectos indeseables
Se han notificado las siguientes reacciones adversas con enalapril en ensayos clínicos y en la experiencia postcomercialización:
Tabla 3. Efectos secundarios de Innovace
* Las tasas de incidencia fueron comparables a las informadas en los grupos de control activo y placebo en los ensayos clínicos.
Notificación de sospechas de reacciones adversas
La notificación de sospechas de reacciones adversas que se produzcan después de la autorización del medicamento es importante, ya que permite un seguimiento continuo de la relación beneficio / riesgo del medicamento. Se ruega a los profesionales sanitarios que notifiquen cualquier sospecha de reacciones adversas a través del sistema nacional de notificación. "Dirección: www. .agenziafarmaco.gov.it / it / responsabili.
04.9 Sobredosis
Se dispone de datos limitados sobre la sobredosis en seres humanos. Las manifestaciones más destacadas son la hipotensión marcada, que comienza aproximadamente seis horas después de la ingestión de los comprimidos, concomitante con el bloqueo del sistema renina-angiotensina y estupor. Los síntomas asociados con una sobredosis de inhibidores de la ECA pueden incluir shock circulatorio, alteraciones electrolíticas, insuficiencia renal, hiperventilación, taquicardia, palpitaciones, bradicardia, mareos, ansiedad y tos. Después de la ingestión de 300 mg y 440 mg de enalapril, se informó que los niveles séricos de enalaprilato eran 100 y 200 veces más altos, respectivamente, que los que se observan típicamente después de dosis terapéuticas.
El tratamiento recomendado en caso de sobredosis es la infusión intravenosa de solución salina. En caso de hipotensión, el paciente debe colocarse en decúbito supino. Si está disponible, se puede considerar el tratamiento con angiotensina II y / o catecolaminas. La ingestión es reciente, tomar medidas para eliminar el maleato de enalapril. (por ejemplo: emesis, lavado gástrico, administración de adsorbentes y sulfato de sodio). Enalaprilato puede eliminarse de la circulación general mediante hemodiálisis (ver sección 4.4). El tratamiento con marcapasos está indicado para la bradicardia refractaria al tratamiento. Los signos vitales, los electrolitos séricos y las concentraciones de creatinina deben controlarse continuamente.
05.0 PROPIEDADES FARMACOLÓGICAS
05.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: inhibidores de la enzima convertidora de angiotensina.
Código ATC: C09A A02.
Innovace (maleato de enalapril) es la sal maleato de enalapril, un derivado de dos aminoácidos, L-alanina y L-prolina. La enzima convertidora de angiotensina (ECA) es una peptidildipeptidasa que cataliza la conversión de angiotensina I en la sustancia que actúa a presión. , angiotensina II. Después de la absorción, enalapril se hidroliza a enalaprilato, que inhibe la ECA. La inhibición de la ECA da como resultado una disminución de los niveles plasmáticos de angiotensina II, lo que conduce a un aumento de la actividad de la renina plasmática (debido a la eliminación de la retroalimentación negativa ejercida sobre la liberación de renina) y una disminución en la secreción de aldosterona.
La ECA es idéntica a la quinasa II, por lo que Enapren también puede bloquear la degradación de la bradicinina, un potente péptido vasodilatador, cuya función sobre los efectos terapéuticos de Enapren aún no se ha aclarado.
Mecanismo de acción
Aunque el mecanismo por el cual Innovace reduce la presión arterial parece ser principalmente la supresión del sistema renina-angiotensina-aldosterona, Innovace también es eficaz en pacientes con hipertensión con niveles bajos de renina.
Efectos farmacodinámicos
La administración de Innovace a pacientes hipertensos da como resultado una reducción de la presión arterial tanto en decúbito supino como en bipedestación sin un aumento significativo de la frecuencia cardíaca.
La hipotensión postural sintomática es infrecuente. En algunos pacientes, pueden ser necesarias varias semanas de tratamiento para lograr una reducción óptima de la presión arterial. La interrupción brusca de Innovace no se ha asociado con un aumento rápido de la presión arterial.
La inhibición eficaz de la actividad de la enzima convertidora suele comenzar de 2 a 4 horas después de la administración oral de una dosis única de enalapril. El inicio de la actividad antihipertensiva suele observarse después de una hora y la actividad máxima se alcanza dentro de las 4 a 6 horas posteriores a la administración. La duración del efecto depende de la dosis, sin embargo, a la dosis recomendada, los efectos hemodinámicos y antihipertensivos continúan durante al menos 24 horas.
En estudios hemodinámicos realizados en pacientes con hipertensión esencial, la reducción de la presión arterial se asoció con una reducción de la resistencia arterial periférica con aumento del gasto cardíaco y cambio mínimo o nulo en la frecuencia cardíaca. Hubo un aumento en el flujo sanguíneo renal después de la administración de Innovace; la tasa de filtración glomerular no se modificó. No hubo signos de retención de agua o sodio. Sin embargo, en pacientes con una tasa de filtración glomerular baja antes del tratamiento, esta generalmente mostró un aumento.
Se han observado disminuciones en la albuminuria, la excreción urinaria de IgG y la proteinuria total en estudios clínicos a corto plazo en pacientes renales diabéticos y no diabéticos después de la administración de enalapril.
Cuando se coadministra un diurético tiazídico con Innovace, el efecto reductor de la presión arterial es al menos aditivo. Innovace puede reducir o prevenir el desarrollo de hipopotasemia inducida por tiazidas.
En pacientes con insuficiencia cardíaca tratados con digitálicos y diuréticos, el tratamiento con tabletas o inyectables de Innovace se ha asociado con una disminución de la resistencia periférica y la presión arterial. El gasto cardíaco aumentó mientras que la frecuencia cardíaca disminuyó (generalmente elevada en pacientes con insuficiencia cardíaca). La presión de enclavamiento capilar pulmonar también disminuyó. La tolerancia al ejercicio y la gravedad de la insuficiencia cardíaca, medidas según los criterios de la New York Heart Association, han mejorado. Estas acciones persistieron durante la terapia crónica.
En pacientes con insuficiencia cardíaca leve o moderada, enalapril ralentizó la progresión de la dilatación / agrandamiento del corazón y la insuficiencia cardíaca, como lo demuestra la reducción de los volúmenes sistólico y telediastólico del ventrículo izquierdo y la mejora de la fracción de eyección.
Doble bloqueo del sistema renina-angiotensina-aldosterona (RAAS)
Dos grandes ensayos controlados aleatorios (ONTARGET (ONTARGET (Telmisartan solo en curso y en combinación con Ramipril Global Endpoint Trial) y VA Nephron-D (The Veterans Affairs Nephropathy in Diabetes)) han examinado el uso de la combinación de un inhibidor de la ECA con un antagonista de la receptor de angiotensina II.
ONTARGET fue un estudio realizado en pacientes con antecedentes de enfermedad cardiovascular o cerebrovascular o diabetes mellitus tipo 2 asociada con evidencia de daño orgánico. VA NEPHRON-D fue un estudio realizado en pacientes con diabetes mellitus tipo 2 y nefropatía diabética.
Estos estudios no demostraron ningún efecto beneficioso significativo sobre los resultados renales y / o cardiovasculares y la mortalidad, mientras que se observó un mayor riesgo de hiperpotasemia, lesión renal aguda y / o hipotensión en comparación con la monoterapia.
Estos resultados también son relevantes para otros inhibidores de la ECA y antagonistas del receptor de angiotensina II, dadas sus propiedades farmacodinámicas similares.
Por tanto, los inhibidores de la ECA y los antagonistas de los receptores de la angiotensina II no deben utilizarse simultáneamente en pacientes con nefropatía diabética.
ALTITUDE (Aliskiren Trial in Type 2 Diabetes Using Cardiovascular and Renal Disease Endpoints) fue un estudio destinado a verificar la ventaja de agregar aliskiren a la terapia estándar de un inhibidor de la ECA o un antagonista del receptor de angiotensina II en pacientes con diabetes mellitus tipo 2 y enfermedad renal crónica. , enfermedad cardiovascular, o ambas. El estudio se terminó antes de tiempo debido a un mayor riesgo de eventos adversos. La muerte cardiovascular y el accidente cerebrovascular fueron numéricamente más frecuentes en el grupo de aliskiren que en el grupo de placebo y los eventos adversos y eventos adversos graves de interés , hipotensión y disfunción renal) se notificaron con mayor frecuencia en el grupo de aliskiren que en el grupo de placebo.
Eficacia clínica y seguridad
Un estudio multicéntrico, aleatorizado, doble ciego y controlado con placebo (Estudio de prevención SOLVD) examinó una población con disfunción ventricular izquierda (FEVI
Un estudio multicéntrico, aleatorizado, doble ciego y controlado con placebo (estudio de tratamiento SOLVD) examinó una población con insuficiencia cardíaca congestiva debido a disfunción sistólica (fracción de eyección de infarto de miocardio 23% (IC del 95%, 11-34%; 20% de pangina inestable). pectoris (IC del 95%, 9-29%; p
Población pediátrica
Existe una experiencia limitada de uso en pacientes pediátricos hipertensos mayores de 6 años. En un ensayo clínico de 110 pacientes pediátricos hipertensos de 6 a 16 años con un peso corporal ≥ 20 kg y una tasa de filtración glomerular> 30 ml / min / 1,73 m2, a pacientes con peso corporal
05.2 Propiedades farmacocinéticas
Absorción
El enalapril oral se absorbe rápidamente; las concentraciones séricas máximas de enalapril se alcanzan en una hora después de la administración. Según la cantidad excretada en la orina, la tasa de absorción de enalapril de los comprimidos de Innovace es aproximadamente del 60%. La absorción de Innovace oral no se ve afectada por la presencia de alimentos en el tracto gastrointestinal.
Después de la absorción, el enalapril oral se hidroliza rápida y ampliamente a enalaprilato, un potente inhibidor de la enzima convertidora de angiotensina. La concentración sérica máxima de enalaprilato se produce aproximadamente 4 horas después de una dosis oral de enalapril. La vida media de acumulación efectiva de enalaprilato después de múltiples dosis orales de enalapril es de 11 horas. En individuos con función renal normal, las concentraciones séricas de enalaprilato en estado estacionario se alcanzaron después de 4 días de tratamiento.
Distribución
Dentro de un intervalo de concentración terapéuticamente relevante, el enalaprilato unido a proteínas plasmáticas humanas no supera el 60%.
Biotransformación
Excepto por la conversión a enalaprilat, no hay evidencia de metabolismo significativo de enalapril.
Eliminación
Enalaprilat se elimina fundamentalmente por vía renal.Los principales compuestos en la orina son enalaprilato, que representa el 40% de la dosis, y enalapril inalterado (aproximadamente el 20%).
Daño en el riñón
La exposición a enalapril y enalaprilat aumentó en pacientes con insuficiencia renal. En pacientes con insuficiencia renal leve a moderada (aclaramiento de creatinina 40-60 ml / min), el AUC de enalaprilato en el estadio estable fue dos veces mayor que en pacientes con insuficiencia renal normal. función renal después de la administración de 5 mg una vez al día. En pacientes con
daño renal severo (aclaramiento de creatinina
Niños y adolescentes
Se realizó un estudio farmacocinético de dosis múltiples en 40 pacientes pediátricos hipertensos masculinos y femeninos de 2 meses a ≤ 16 años después de la administración oral diaria de 0,07 a 0,14 mg / kg de maleato de enalapril. No hubo diferencias importantes en la farmacocinética de enalaprilato en niños en comparación con los datos históricos en adultos. Los datos indican un aumento en el AUC (dosis normalizada para el peso corporal) con el aumento de la edad; sin embargo, no se observa ningún aumento en el AUC cuando los datos se normalizan por área de superficie corporal. En estado estacionario, la vida media de acumulación efectiva media de enalaprilato fue de 14 horas.
Hora de la comida
Después de una dosis oral única de 20 mg en cinco mujeres en posparto, el nivel máximo medio de enalapril en la leche fue de 1,7 mcg / L (rango de 0,54 a 5,9 mcg / L) 4 a 6 horas después de la dosis. El nivel máximo medio de enalaprilato fue de 1,7 mcg / L (rango de 1,2 a 2,3 mcg / L); los picos se produjeron en diferentes momentos durante el período de 24 horas. Utilizando datos de los niveles máximos de leche, la ingesta máxima estimada de un lactante exclusivamente amamantado sería aproximadamente el 0,16% de la dosis materna ajustada al peso.
Una mujer que había tomado 10 mg diarios de enalapril oral durante 11 meses tuvo niveles máximos de enalapril en la leche de 2 mcg / L 4 horas después de una dosis y niveles máximos de enalaprilat de 0,75 mcg / L aproximadamente 9 horas después de la dosis. La cantidad total de enalapril y enalaprilat medida en la leche durante el período de 24 horas fue de 1,44 mcg / L y 0,63 mcg / L, respectivamente.
Los niveles de enalaprilato en la leche no fueron medibles (
05.3 Datos preclínicos sobre seguridad
Los datos de seguridad no clínicos no destacan ningún peligro especial para los seres humanos según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas, genotoxicidad y potencial carcinogénico. Los estudios de toxicidad reproductiva sugieren que enalapril no tiene ningún efecto sobre la fertilidad y el rendimiento reproductivo en la rata y no es teratogénico. En un estudio en el que se administró el fármaco a ratas hembras antes del apareamiento hasta la gestación, hubo un aumento en la tasa de muertes en las crías lactantes. Se ha demostrado que el compuesto atraviesa la barrera placentaria y se excreta en la leche materna. Se ha demostrado que los inhibidores de la enzima convertidora de angiotensina, como clase, son fetotóxicos (causan daño fetal y / o muerte) cuando se administran durante el segundo o tercer trimestre.
06.0 INFORMACIÓN FARMACÉUTICA
06.1 Excipientes
Hidrógeno de sodio carbonatado
Maicena
Almidón de maíz pregelatinizado
Estearato de magnesio
Lactosa monohidrato
Óxido de hierro rojo (E172): solo tabletas de 20 mg
Óxido de hierro amarillo (E172): solo comprimidos de 20 mg
06.2 Incompatibilidad
Irrelevante.
06.3 Período de validez
2 años.
06.4 Precauciones especiales de conservación
No conservar a temperatura superior a 25 ° C. Conservar en el embalaje original para protegerlo de la humedad.
06.5 Naturaleza del envase primario y contenido del envase.
Los comprimidos de Innovace 5 mg están disponibles en blísteres de aluminio que contienen 2, 14, 20, 28, 28 x 1, 30, 49 x 1, 50, 60, 98 o 100 comprimidos.
Los comprimidos de Innovace 20 mg están disponibles en blísteres de aluminio que contienen 10, 14, 20, 28, 28 x 1, 30, 49 x 1, 50, 56, 60, 84, 90, 98, 100 o 500 comprimidos.
Es posible que no se comercialicen todos los tamaños de envases.
06.6 Instrucciones de uso y manipulación
Sin instrucciones especiales.
07.0 TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
MERCK SHARP & DOHME LIMITED
Hertford Road, Hoddesdon
Hertfordshire, Gran Bretaña
08.0 NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN
28 comprimidos 5 mg 025682042
14 comprimidos 20 mg 025682028
28 comprimidos 20 mg 025682079
09.0 FECHA DE LA PRIMERA AUTORIZACIÓN O RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de la primera autorización:
Tabletas Innovace de 5 mg: 27 de abril de 1987
Tabletas Innovace de 20 mg: 12 de marzo de 1985
Fecha de la última renovación: 17 de noviembre de 2010
10.0 FECHA DE REVISIÓN DEL TEXTO
Junio de 2015