Ingredientes activos: exenatida
Bydureon 2 mg polvo y disolvente para suspensión inyectable de liberación prolongada
Prospecto fuente: AIFA (Agencia Italiana de Medicamentos). Contenido publicado en enero de 2016. Es posible que la información presente no esté actualizada.
Para tener acceso a la versión más actualizada, es recomendable acceder al sitio web de la AIFA (Agencia Italiana de Medicamentos). Descargo de responsabilidad e información útil.
01.0 NOMBRE DEL MEDICAMENTO -
BYDUREON 2 MG POLVO Y DISOLVENTE PARA SUSPENSIÓN INYECTABLE DE LIBERACIÓN PROLONGADA
02.0 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA -
Cada vial contiene 2 mg de exenatida.
Para consultar la lista completa de excipientes, ver sección 6.1.
03.0 FORMA FARMACÉUTICA -
Polvo de liberación prolongada y disolvente para suspensión inyectable.
Polvo: Polvo de color blanco a blanquecino.
Disolvente: solución transparente, incolora, de color amarillo claro a marrón claro.
04.0 INFORMACIÓN CLÍNICA -
04.1 Indicaciones terapéuticas -
Bydureon está indicado para el tratamiento de la diabetes mellitus tipo 2 en combinación con:
• Metformina
• Sulfonilurea
• Tiazolidinediona
• Metformina y sulfonilurea
• Metformina y tiazolidindiona
en pacientes adultos que no han logrado un control glucémico adecuado con la dosis máxima tolerada de estas terapias orales.
04.2 Posología y forma de administración -
Dosis
La dosis recomendada es de 2 mg de exenatida una vez a la semana.
Los pacientes que cambian de exenatida de liberación inmediata (Byetta) a exenatida de liberación prolongada (Bydureon) pueden experimentar aumentos transitorios en las concentraciones de glucosa en sangre que generalmente mejoran dentro de las dos primeras semanas después del inicio del tratamiento.
Cuando se agrega exenatida de liberación prolongada a la terapia existente con metformina y / o tiazolidinediona, se puede mantener la dosis continua de metformina y / o tiazolidinediona. Cuando se añade exenatida de liberación prolongada al tratamiento con una sulfonilurea, se debe considerar una reducción de la dosis de sulfonilurea para reducir el riesgo de hipoglucemia (ver sección 4.4).
La exenatida de liberación prolongada debe administrarse una vez a la semana, el mismo día de cada semana. El día de la administración semanal se puede cambiar si es necesario siempre que la siguiente dosis se administre al menos un día después (24 horas). La exenatida de liberación prolongada se puede administrar en cualquier momento del día, independientemente de las comidas.
Si se olvida una dosis, debe administrarse lo antes posible. Para la siguiente inyección, los pacientes pueden volver al día de inyección elegido, sin embargo, solo se debe administrar una inyección en un plazo de 24 horas.
El uso de exenatida de liberación prolongada no requiere un autocontrol adicional de los niveles de glucosa en sangre, sin embargo, puede ser necesario un autocontrol de los niveles de glucosa en sangre para ajustar la dosis de sulfonilurea.
Si se inicia un tratamiento hipoglucemiante diferente después de la interrupción de la exenatida de liberación prolongada, se debe prestar atención a la exenatida de liberación prolongada de liberación prolongada (ver sección 5.2).
Poblaciones especiales
Personas mayores
No se requieren ajustes de dosis en función de la edad, sin embargo, como la función renal generalmente disminuye con la edad, se debe considerar la función renal del paciente (ver pacientes con insuficiencia renal). La experiencia clínica en pacientes mayores de 75 años es muy limitada (ver sección 5.2).
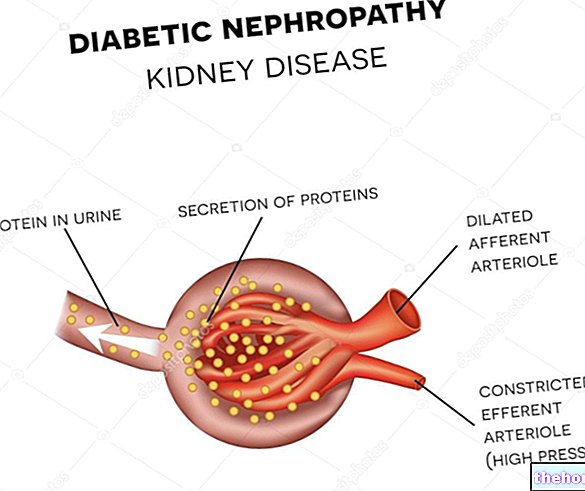
Daño en el riñón
No se requieren ajustes de dosis en pacientes con insuficiencia renal leve (aclaramiento de creatinina de 50 a 80 ml / min). La experiencia clínica en pacientes con insuficiencia renal moderada (aclaramiento de creatinina de 30 a 50 ml / min) es muy limitada (ver sección 5.2) No se recomienda exenatida de liberación prolongada en estos pacientes.
No se recomienda exenatida de liberación prolongada en pacientes con enfermedad renal en etapa terminal o insuficiencia renal grave (aclaramiento de creatinina
Deterioro hepático
No se requieren ajustes de dosis para pacientes con insuficiencia hepática (ver sección 5.2).
Población pediátrica
No se ha establecido todavía la seguridad y eficacia de exenatida de liberación prolongada en niños y adolescentes menores de 18 años. Los datos actualmente disponibles se describen en la sección 5.2, pero no se puede hacer una recomendación posológica.
Método de administración
La exenatida de liberación prolongada es para autoadministración por parte del paciente.Cada kit es para uso de una sola persona y es para un solo uso.
Antes de iniciar el tratamiento con exenatida de liberación prolongada, se recomienda encarecidamente que un profesional sanitario instruya a los pacientes y a los profesionales no sanitarios.
Las "Instrucciones para el usuario" adjuntas al paquete deben seguirse cuidadosamente.
Cada dosis debe administrarse mediante inyección subcutánea en el abdomen, el muslo o la parte superior de la espalda de los brazos inmediatamente después de la suspensión del polvo en el disolvente.
Para obtener instrucciones sobre cómo suspender el medicamento antes de la administración, ver sección 6.6 e "Instrucciones para el usuario".
04.3 Contraindicaciones -
Hipersensibilidad al principio activo oa alguno de los excipientes incluidos en la sección 6.1.
04.4 Advertencias especiales y precauciones de uso apropiadas -
La exenatida de liberación prolongada no debe usarse en pacientes con diabetes mellitus tipo 1 o para el tratamiento de la cetoacidosis diabética.
La exenatida de liberación prolongada no debe administrarse mediante inyección intravenosa o intramuscular.
Daño en el riñón
En pacientes con enfermedad renal en etapa terminal sometidos a diálisis, dosis únicas de exenatida de liberación inmediata provocaron un aumento en la frecuencia y gravedad de las reacciones adversas gastrointestinales; por lo tanto, no se recomienda exenatida de liberación prolongada en pacientes con enfermedad renal en etapa terminal o insuficiencia renal grave (aclaramiento de creatinina
Ha habido casos poco frecuentes de insuficiencia renal con exenatida, que incluyen aumento de la creatinina, insuficiencia renal, empeoramiento de la insuficiencia renal crónica e insuficiencia renal aguda, que a veces requirieron hemodiálisis. Algunos de estos eventos ocurrieron en pacientes que tuvieron eventos capaces de alterar el estado de hidratación, incluyendo náuseas, vómitos y / o diarrea y / o que estaban siendo tratados con medicamentos que se sabe que alteran el estado de hidratación / función renal. Los medicamentos administrados concomitantemente incluyeron inhibidores de la enzima convertidora de angiotensina, antagonistas de la angiotensina II, antiinflamatorios no esteroideos y diuréticos, discontinuación de los agentes potencialmente responsables de estos eventos, incluida exenatida.
Enfermedad gastrointestinal severa
No se ha estudiado la exenatida de liberación prolongada en pacientes con enfermedad gastrointestinal grave, incluida la gastroparesia. Su uso se asocia comúnmente con reacciones adversas gastrointestinales que incluyen náuseas, vómitos y diarrea. Por tanto, no se recomienda el uso de exenatida de liberación prolongada en pacientes con enfermedad gastrointestinal grave.
Pancreatitis aguda
El uso de agonistas del receptor de GLP-1 se ha asociado con el riesgo de desarrollar pancreatitis aguda. Se han notificado casos de pancreatitis aguda de forma espontánea con exenatida de liberación prolongada. Se ha observado resolución de la pancreatitis con el tratamiento de apoyo, pero se han notificado casos muy raros. Se han notificado casos de pancreatitis necrosante o hemorrágica y / o muerte. Se debe informar a los pacientes del síntoma característico de la pancreatitis aguda: dolor abdominal intenso y persistente. Si se sospecha pancreatitis, se debe suspender la exenatida de liberación prolongada; si se confirma la pancreatitis aguda , no se debe reanudar el tratamiento con exenatida de liberación prolongada. Se debe tener precaución en pacientes con antecedentes de pancreatitis.
Medicamentos utilizados al mismo tiempo.
No se ha estudiado el uso de exenatida de liberación prolongada en combinación con insulina, derivados de D-fenilalanina (meglitinidas), inhibidores de la alfa-glucosidasa, inhibidores de la dipeptidil peptidasa-4 u otros agonistas del receptor de GLP-1. No se ha estudiado y no se recomienda el uso de exenatida de liberación prolongada en combinación con exenatida de liberación inmediata.
Interacciones con warfarina
Durante el uso concomitante de warfarina y exenatida, se han notificado de forma espontánea casos de aumento del INR (índice internacional normalizado), a veces asociado con hemorragias (ver sección 4.5).
Hipoglucemia
Cuando se utilizó exenatida de liberación prolongada en combinación con una sulfonilurea en ensayos clínicos, aumenta el riesgo de hipoglucemia. Además, en los ensayos clínicos, los pacientes con insuficiencia renal leve que recibieron tratamiento en combinación con una sulfonilurea tuvieron una mayor incidencia de hipoglucemia en comparación con los pacientes con función renal normal. Para reducir el riesgo de hipoglucemia asociado con el uso de una sulfonilurea, se debe considerar una reducción de la dosis de sulfonilurea.
Pérdida de peso rápida
Se ha observado una rápida pérdida de peso> 1,5 kg por semana en pacientes tratados con exenatida. Una pérdida de peso de esta magnitud puede tener consecuencias perjudiciales. Se debe vigilar a los pacientes con pérdida de peso rápida para detectar signos y síntomas de colelitiasis.
Interrupción del tratamiento.
Después de la interrupción, el efecto de liberación prolongada de exenatida puede continuar a medida que los niveles plasmáticos de exenatida disminuyen durante 10 semanas. En consecuencia, se debe considerar la elección de otros medicamentos y la elección de la dosis, ya que las reacciones adversas pueden continuar y la eficacia puede persistir, en al menos en parte, hasta que disminuyan los niveles de exenatida.
Excipientes
Contenido de sodio: este medicamento contiene menos de 1 mmol de sodio (23 mg) por dosis, es decir, esencialmente "exento de sodio".
04.5 Interacciones con otros medicamentos y otras formas de interacción -
Sulfonilureas
La dosis de una sulfonilurea puede requerir un ajuste debido al aumento del riesgo de hipoglucemia asociado con el tratamiento con sulfonilurea (ver secciones 4.2 y 4.4).
Vaciamiento gástrico
Los resultados de un estudio que utilizó paracetamol como marcador del vaciamiento gástrico sugieren que el efecto de la exenatida de liberación prolongada sobre la desaceleración del vaciamiento gástrico es menor y no se espera que provoque reducciones clínicamente significativas en la velocidad y el grado de absorción del fármaco administrado simultáneamente por vía oral. Por tanto, no se requieren ajustes de dosis para medicamentos sensibles al vaciamiento gástrico retardado.
Cuando, después de 14 semanas de tratamiento con exenatida de liberación prolongada, se administraron comprimidos de 1000 mg de paracetamol, independientemente de las comidas, no se observaron cambios significativos en el AUC de paracetamol en comparación con el período de control. 16% (en ayunas) y 5% (con alimentos) y el tmáx aumentó de aproximadamente 1 hora en el período de control a 1,4 horas (en ayunas) y 1,3 horas (con alimentos).
Los siguientes estudios de interacción se realizaron utilizando exenatida de liberación inmediata 10 mcg pero no exenatida de liberación prolongada:
Warfarina
Cuando se administró warfarina 35 minutos después de la exenatida de liberación inmediata, se observó un retraso en el tmáx de aproximadamente 2 horas. No se observaron efectos clínicamente significativos sobre la Cmáx o el AUC. Se ha notificado de forma espontánea un aumento del valor de INR durante el uso concomitante de warfarina y exenatida de liberación prolongada. Se debe verificar el INR al inicio del tratamiento con exenatida. Liberación prolongada en pacientes que reciben warfarina y / o exenatida de liberación prolongada. Derivados cumarínicos (ver secciones 4.4 y 4.8).
Inhibidores de la hidroximetilglutaril coenzima A (HMG CoA) reductasa
El AUC y la Cmax de lovastatina disminuyeron aproximadamente un 40% y un 28%, respectivamente, y el tmax se retrasó aproximadamente 4 horas cuando se administró exenatida de liberación inmediata en combinación con una dosis única de lovastatina (40 mg) en comparación con lovastatina administrada sola. En los ensayos clínicos de 30 semanas controlados con placebo con exenatida de liberación inmediata, el uso concomitante de exenatida con inhibidores de la HMG CoA reductasa no se asoció con un cambio correspondiente en el perfil de lípidos (ver párrafo 5.1). No se requiere un ajuste de dosis predeterminado; sin embargo, los perfiles de lípidos deben controlarse adecuadamente.
Digoxina y lisinopril
No se observaron efectos clínicamente relevantes sobre la Cmáx o el AUC en los estudios de interacción del efecto de exenatida de liberación inmediata sobre digoxina y lisinopril; sin embargo, se observó un retraso en tmax de aproximadamente 2 horas.
Etinilestradiol y levonorgestrel
La administración de un anticonceptivo oral combinado (30 microgramos de etinilestradiol más 150 microgramos de levonorgestrel) una hora antes de la exenatida de liberación inmediata no modificó el AUC, Cmax ni Cmin del etinilestradiol o levonorgestrel. La administración del anticonceptivo oral combinado 35 minutos después de exenatida no cambió el AUC, pero dio como resultado una reducción del 45% en la Cmáx del etinilestradiol y una reducción del 27-41% en la Cmáx del levonorgestrel y un retraso de 2-4 horas en el tmáx debido a un vaciamiento gástrico más lento. La reducción de la Cmáx tiene una relevancia clínica limitada y no es necesario ajustar la dosis de los anticonceptivos orales.
Población pediátrica
Los estudios de interacción con exenatida solo se han realizado en adultos.
04.6 Embarazo y lactancia -
Mujeres en edad fértil
Debido al largo período de eliminación de exenatida de liberación prolongada, las mujeres en edad fértil deben utilizar métodos anticonceptivos durante el tratamiento con exenatida de liberación prolongada. La exenatida de liberación prolongada debe suspenderse al menos 3 meses antes del embarazo planificado.
El embarazo
Los datos sobre el uso de exenatida de liberación prolongada en mujeres embarazadas no son adecuados. Los estudios en animales han mostrado toxicidad para la reproducción (ver sección 5.3). Se desconoce el riesgo potencial para los seres humanos. Se recomienda el uso de insulina.
Hora de la comida
Se desconoce si exenatida se excreta en la leche materna. La exenatida de liberación prolongada no debe usarse durante la lactancia.
Fertilidad
No se han realizado estudios de fertilidad en humanos.
04.7 Efectos sobre la capacidad para conducir y utilizar máquinas.
La exenatida de liberación prolongada tiene efectos menores sobre la capacidad para conducir o utilizar máquinas. Cuando se utiliza exenatida de liberación prolongada en combinación con una sulfonilurea, se debe advertir a los pacientes que tomen las precauciones necesarias para evitar la aparición de una reacción hipoglucemiante mientras conducen un vehículo o utilizan maquinaria.
04.8 Efectos indeseables -
Resumen del perfil de seguridad
Las reacciones adversas más frecuentes fueron principalmente gastrointestinales (náuseas, que fue la reacción más frecuente y asociada al inicio del tratamiento y disminuyó con la continuación del tratamiento, y diarrea), lugar de inyección (picor, nódulos, eritema), hipoglucemia (con una sulfonilurea) y dolor de cabeza. . La mayoría de las reacciones adversas asociadas con el uso de exenatida de liberación prolongada fueron de intensidad leve a moderada.
Desde que se comercializó exenatida de liberación inmediata, se han notificado casos de pancreatitis aguda con una frecuencia desconocida y, con poca frecuencia, se han notificado casos de insuficiencia renal aguda (ver sección 4.4).
Tabla resumen de reacciones adversas
La frecuencia de las reacciones adversas de liberación prolongada identificadas en los ensayos clínicos y las notificaciones espontáneas (no observadas en los ensayos clínicos, frecuencia no conocida) se resumen a continuación en la Tabla 1.
La fuente de datos de los ensayos clínicos de exenatida incluye 18 ensayos clínicos controlados con placebo, 21 ensayos clínicos controlados con activos y 2 ensayos clínicos abiertos. Las terapias de fondo incluyeron dieta y ejercicio, metformina, una sulfonilurea, una tiazolidindiona o una combinación de fármacos hipoglucemiantes orales.
Las reacciones se enumeran a continuación bajo los términos de MedDRA según la clasificación de órganos del sistema y la frecuencia absoluta. Las frecuencias se definen como: muy frecuentes (≥1 / 10), frecuentes (≥1 / 100,
Tabla 1: Reacciones adversas de exenatida de liberación prolongada identificadas en estudios clínicos y notificaciones espontáneas.
¹ Incidencia basada en estudios de eficacia y seguridad a largo plazo completados con exenatida de liberación prolongada total n = 2868 (pacientes tratados con sulfonilurea n = 1002).
² Incidencia basada en datos de notificación espontánea con exenatida de liberación prolongada (denominador desconocido).
Descripción de reacciones adversas seleccionadas
Hipoglucemia
La incidencia de hipoglucemia aumentó cuando se utilizó exenatida de liberación prolongada en combinación con una sulfonilurea (24,0% versus 5,4%) (ver sección 4.4). Para reducir el riesgo de hipoglucemia asociado con el uso de una sulfonilurea, se puede considerar la reducción de la dosis de la sulfonilurea (ver secciones 4.2 y 4.4).
La exenatida de liberación prolongada se asoció con una incidencia significativamente menor de episodios hipoglucémicos en comparación con la insulina basal en pacientes que también recibieron tratamiento con metformina (3% versus 19%) y también en pacientes que reciben tratamiento con metformina asociada a sulfonilurea (20% versus 42%).
En los 11 estudios de exenatida de liberación prolongada, la mayoría de los episodios (99,9% n = 649) de hipoglucemia fueron menores y se resolvieron con la administración oral de carbohidratos. Solo un paciente refirió un episodio de hipoglucemia mayor porque tenía un valor de glucosa en sangre bajo (2,2 mmol / L) y requirió asistencia con un tratamiento con carbohidratos por vía oral que resolvió el evento.
Náusea
La reacción adversa notificada con más frecuencia fue náuseas. En los pacientes tratados con exenatida de liberación prolongada, generalmente el 20% notificó al menos un episodio de náuseas en comparación con el 34% de los pacientes tratados con exenatida de liberación inmediata. La mayoría de los episodios de náuseas fueron de leves a moderados. Con la terapia continua, la frecuencia disminuyó en la mayoría de los pacientes que inicialmente tenían náuseas.
La incidencia de interrupción debido a eventos adversos durante el ensayo clínico controlado de 30 semanas fue del 6% en los pacientes tratados con exenatida de liberación prolongada y del 5% en los pacientes tratados con exenatida de liberación inmediata. náuseas y vómitos. La interrupción debido a náuseas o vómitos fue
Reacciones en el lugar de la inyección
Durante los 6 meses de la fase controlada de los estudios, se notificaron reacciones en el lugar de la inyección con mayor frecuencia en pacientes tratados con exenatida de liberación prolongada que en pacientes tratados con comparador (16% versus el rango 2-7%). Estas reacciones en el lugar de la inyección fueron generalmente leves y normalmente no dieron lugar a la retirada de los estudios. Los pacientes pueden recibir tratamiento para aliviar los síntomas mientras continúan el tratamiento. Se debe utilizar un lugar de inyección diferente cada semana para las inyecciones posteriores. En la experiencia postcomercialización, se han notificado casos de abscesos y celulitis en el lugar de la inyección.
En estudios clínicos se han observado con mucha frecuencia pequeños nódulos subcutáneos en el lugar de la inyección, de acuerdo con las propiedades conocidas de las formulaciones de perlas de polímero de poli (D, L-lactida-co-glicólido). La mayoría de los nódulos individuales eran asintomáticos, no interfirieron con la participación en el estudio y se resolvieron en 4-8 semanas.
Inmunogenicidad
De acuerdo con la inmunogenicidad potencial de los fármacos proteicos y peptídicos, los pacientes pueden desarrollar anticuerpos anti-exenatida después del tratamiento con exenatida de liberación prolongada. En la mayoría de los pacientes que desarrollan anticuerpos, el título de anticuerpos disminuye con el tiempo.
La presencia de anticuerpos (títulos altos o bajos) no predice el control de la glucosa en sangre para un paciente individual.
En los ensayos clínicos de exenatida de liberación prolongada, aproximadamente el 45% de los pacientes tenían un título bajo de anticuerpos anti-exenatida al final del estudio. El porcentaje general de pacientes con positividad de anticuerpos fue constante en todos los ensayos clínicos. En general, el nivel de control glucémico (HbA1c) fue comparable al observado en pacientes sin respuesta de anticuerpos. En los estudios de fase 3, en promedio, el 12% de los pacientes tenían un título de anticuerpos más alto. En algunos de ellos, la respuesta glucémica a la exenatida de liberación prolongada estuvo ausente al final del período controlado de los estudios; El 2,6% de los pacientes no mostró mejoría en la glucosa en sangre con títulos de anticuerpos más altos, mientras que el 1,6% no mostró mejoría con anticuerpos negativos.
Los pacientes que han desarrollado anticuerpos anti-exenatida tienden a tener más reacciones en el lugar de la inyección (por ejemplo: enrojecimiento de la piel y picazón), pero, por otro lado, experimentan eventos adversos de incidencia y tipo similares a los pacientes que no los padecen. desarrollado anticuerpos anti-exenatida.
Para los pacientes tratados con exenatida de liberación prolongada, la incidencia de reacciones potencialmente inmunogénicas en el lugar de la inyección (más comúnmente prurito con o sin eritema) durante el estudio de 30 semanas y los dos estudios de 26 semanas fue aproximadamente del 9%. con menos frecuencia en pacientes con anticuerpos negativos (4%) que en pacientes con anticuerpos positivos (13%), con una mayor incidencia en aquellos con títulos de anticuerpos más altos.
El examen de muestras positivas para anticuerpos no mostró reactividad cruzada significativa con péptidos endógenos similares (glucagón o GLP-1).
Pérdida de peso rápida
En un estudio clínico de 30 semanas, aproximadamente el 3% de los pacientes (n = 4/148) tratados con exenatida de liberación prolongada experimentaron al menos un período de tiempo de rápida pérdida de peso (la pérdida de peso corporal detectada entre 2 controles consecutivos en el estudio fue superior a 1,5 kg / semana).
Aumento de la frecuencia cardíaca
Se observó un aumento medio de la frecuencia cardíaca (FC) de 2,6 latidos por minuto (lpm) con respecto al valor inicial (74 lpm) en los estudios clínicos combinados de exenatida de liberación prolongada. El quince por ciento de los pacientes tratados con exenatida de liberación prolongada tuvieron aumentos medios en la FC de ≥10 lpm; aproximadamente del 5% al 10% de los sujetos dentro de los otros grupos de tratamiento tuvieron aumentos medios en la FC ≥10 lpm.
Notificación de sospechas de reacciones adversas
La notificación de sospechas de reacciones adversas que se produzcan después de la autorización del medicamento es importante, ya que permite un seguimiento continuo de la relación beneficio / riesgo del medicamento. Se invita a los profesionales sanitarios a notificar cualquier sospecha de reacciones adversas a través del sistema nacional de notificación en la dirección www. .agenziafarmaco.gov.it / it / responsabili.
04.9 Sobredosis -
Los efectos de la sobredosis de exenatida (basados en estudios clínicos de exenatida de liberación inmediata) incluyen náuseas intensas, vómitos intensos y descenso rápido de la glucosa en sangre. En caso de sobredosis, se debe iniciar un tratamiento de soporte adecuado en función de los signos y síntomas clínicos experimentados por el paciente.
05.0 PROPIEDADES FARMACOLÓGICAS -
05.1 "Propiedades farmacodinámicas -
Grupo farmacoterapéutico: Medicamentos utilizados en diabetes, otros hipoglucemiantes, excluidas las insulinas.
Código ATC: A10BX04.
Mecanismo de acción
La exenatida es un agonista del receptor del péptido 1 similar al glucagón (GLP-1) que exhibe numerosas acciones antihiperglucémicas del péptido 1 similar al glucagón (GLP-1). La secuencia de aminoácidos de exenatida se superpone parcialmente a la del GLP-1 humano. Exenatida mostró in vitro para unirse al receptor de GLP-1 humano y activarlo con un mecanismo de acción mediado por AMP cíclico y / u otras vías de señalización intracelular.
La exenatida aumenta la secreción de insulina de las células beta pancreáticas de manera dependiente de la glucosa. A medida que desciende el azúcar en sangre, la secreción de insulina se ralentiza. Cuando se utilizó exenatida en combinación con metformina y / o tiazolidinediona, no se observó un aumento en la incidencia de hipoglucemia en comparación con placebo en combinación con metformina y / o tiazolidinediona, esto puede deberse a este mecanismo insulinotrópico dependiente de la glucosa (ver párrafo 4.4). .
La exenatida suprime la secreción de glucagón, que se sabe que está inapropiadamente elevada en pacientes con diabetes tipo 2. Las concentraciones más bajas de glucagón dan como resultado una disminución de la producción de glucosa hepática. Sin embargo, exenatida no altera la respuesta normal del glucagón ni otras respuestas hormonales a la hipoglucemia.
La exenatida ralentiza el vaciado gástrico y, en consecuencia, reduce la velocidad a la que la glucosa introducida con la comida aparece en la circulación.
Se ha demostrado que la administración de exenatida reduce la ingesta de alimentos como resultado de la disminución del apetito y el aumento de la saciedad.
Efectos farmacodinámicos
La exenatida mejora el control glucémico a través de sus efectos prolongados sobre el ayuno y la disminución de la glucosa en sangre posprandial en pacientes con diabetes tipo 2. A diferencia del GLP-1 endógeno, la exenatida de liberación prolongada tiene un perfil farmacocinético y farmacodinámico en hombres apropiado para una administración una vez a la semana.
Un estudio farmacodinámico con exenatida ha demostrado en pacientes con diabetes tipo 2 (n = 13) una restauración de la primera fase de secreción de insulina y una mejora de la segunda fase de secreción de insulina en respuesta a la administración de un bolo intravenoso de glucosa.
Eficacia clínica y seguridad
Los resultados de los ensayos clínicos a largo plazo de exenatida de liberación prolongada se presentan a continuación; En estos estudios participaron 1628 sujetos (804 tratados con exenatida de liberación prolongada), 54% hombres y 46% mujeres, 281 sujetos (141 tratados con exenatida de liberación prolongada) tenían ≥65 años.
Control Glicémico
En dos estudios, se comparó exenatida de liberación prolongada 2 mg una vez a la semana con exenatida de liberación inmediata 5 mcg dos veces al día durante 4 semanas, seguida de exenatida de liberación inmediata 10 mcg dos veces al día. Un estudio duró 24 semanas (n = 252) y el otro estudio duró 30 semanas (n = 295) y fue seguido de una fase de extensión abierta en la que todos los pacientes fueron tratados con 2 mg de exenatida de liberación prolongada una vez por semana durante un período de tiempo. 22 semanas adicionales (n = 243) En ambos estudios, las reducciones de HbA1c fueron evidentes en ambos grupos de tratamiento desde la primera medición de HbA1c (después de 4 o 6 semanas) después del inicio del tratamiento.
La exenatida de liberación prolongada resultó en una reducción estadísticamente significativa de la HbA1c en comparación con los pacientes que recibieron exenatida de liberación inmediata (Tabla 2).
En ambos estudios se observó un efecto clínicamente relevante sobre la HbA1c en pacientes tratados con exenatida de liberación prolongada y dos veces al día, independientemente del tratamiento antidiabético de base.
Más pacientes tratados con exenatida de liberación prolongada que pacientes tratados con exenatida de liberación inmediata lograron una reducción de HbA1c ≤7% o
Los pacientes tratados con exenatida de liberación prolongada y de liberación inmediata lograron una reducción del peso corporal con respecto al valor inicial, aunque las diferencias entre los dos grupos de tratamiento no fueron significativas.
Se observaron reducciones adicionales en la HbA1c y una reducción de peso sostenida a lo largo del tiempo durante al menos 52 semanas en pacientes que completaron tanto el estudio controlado de 30 semanas como el estudio de extensión no controlado. Pacientes evaluables que cambiaron de exenatida a liberar exenatida de liberación prolongada (n = 121 ) logró la misma mejora en la HbA1c de -2,0% al final de las 22 semanas de extensión desde el valor inicial que los pacientes tratados con exenatida de liberación prolongada durante 52 semanas.
Tabla 2: Resultados de dos estudios de exenatida de liberación prolongada versus exenatida de liberación inmediata en combinación con dieta y ejercicio solamente, metformina y / o sulfonilurea y metformina y / o tiazolidinediona (muestra del paciente por intención de tratar)
ES = error estándar, CI = intervalo de confianza, * p
Se realizó un estudio de 26 semanas en el que se compararon 2 mg de exenatida de liberación prolongada con insulina glargina una vez al día. La exenatida de liberación prolongada demostró una mayor variación en la HbA1c que la insulina glargina. En comparación con el tratamiento con insulina glargina, el tratamiento con exenatida de liberación prolongada redujo significativamente el peso corporal medio y se asoció con menos eventos hipoglucémicos (Tabla 3).
Tabla 3: Resultados de un estudio de 26 semanas de exenatida de liberación prolongada versus insulina glargina en combinación con metformina sola o metformina y sulfonilurea (muestra del paciente por intención de tratar)
ES = error estándar, CI = intervalo de confianza, * p
¹ La insulina glargina se midió a la concentración de glucosa objetivo de 4,0-5,5 mmol / L (72-100 mg / dL). La dosis media de insulina glargina al inicio del tratamiento fue de 10,1 UI / día con aumentos de hasta 31,1 UI / día para pacientes tratados con insulina glargina.
Los resultados en la semana 156 fueron consistentes con los reportados previamente en el informe intermedio en la semana 26. El tratamiento con exenatida de liberación prolongada mejoró de manera persistente y significativa el control de la glucemia y el control del peso, en comparación con el tratamiento con insulina glargina. Los resultados de seguridad después de 156 semanas fueron consistentes con los informados a las 26 semanas.
En un estudio doble ciego de 26 semanas de duración, se comparó la exenatida de liberación prolongada con las dosis diarias máximas de sitagliptina y pioglitazona en sujetos que también estaban tomando metformina. Todos los grupos de tratamiento tuvieron una reducción significativa de la HbA1 desde el inicio La exenatida de liberación prolongada demostró superioridad en términos de cambio en la HbA1c desde el inicio sobre la sitagliptina y la pioglitazona.
La exenatida de liberación prolongada demostró una reducción del peso corporal significativamente mayor que la sitagliptina. Los pacientes tratados con pioglitazona tuvieron un aumento de peso corporal (Tabla 4).
Tabla 4: Resultados de un estudio de 26 semanas de exenatida de liberación prolongada versus sitagliptina e versus pioglitazona en combinación con metformina (muestra del paciente por intención de tratar)
ES = error estándar, CI = intervalo de confianza, * p
Peso corporal
En todos los estudios de exenatida de liberación prolongada se observó una reducción del peso corporal con respecto al valor inicial. Esta reducción en el peso corporal se observó en pacientes tratados con exenatida de liberación prolongada independientemente de si se produjeron náuseas, aunque la reducción fue mayor en el grupo de náuseas (reducción media de -2,9 kg a -5,2 kg). Kg en presencia de náuseas en comparación con una reducción media de -2,2 kg a -2,9 kg sin náuseas).
La proporción de pacientes que tuvieron una reducción tanto del peso corporal como de la HbA1c osciló entre el 70 y el 79% (la proporción de pacientes que tuvieron una reducción de la HbA1c osciló entre el 88% y el 96%).
Glucosa en sangre plasmática / sérica
El tratamiento con exenatida de liberación prolongada dio como resultado reducciones significativas en la glucosa plasmática / sérica en ayunas, estas reducciones se observaron a las 4 semanas. Se observaron reducciones adicionales en las concentraciones posprandiales. La mejora de la glucosa plasmática / sérica en ayunas se mantuvo durante 52 semanas.
Función de las células beta
Los estudios clínicos con exenatida de liberación prolongada han indicado una mejora en la función de las células beta, utilizando métodos de medición como la "evaluación del modelo de homeostasis" (HOMA-B). La duración del efecto sobre la función de las células beta se mantuvo durante 52 semanas.
Presión arterial
Se observó una reducción de la presión arterial sistólica (de 2,9 mmHg a 4,7 mmHg) en los estudios de exenatida de liberación prolongada. En un estudio de comparación con exenatida de liberación inmediata a las 30 semanas, tanto la exenatida de liberación prolongada como la de liberación inmediata redujeron significativamente la presión arterial sistólica desde el valor inicial (4,7 ± 1,1 mmHg y 3,4 ± 1,1 mmHg respectivamente) y la diferencia entre los tratamientos no fue significativa. La mejora de la presión arterial se mantuvo durante 52 semanas.
Lípidos en ayunas
La exenatida de liberación prolongada no mostró efectos adversos sobre los parámetros lipídicos.
Población pediátrica
La Agencia Europea de Medicamentos ha aplazado la obligación de presentar los resultados de los estudios con exenatida de liberación prolongada en uno o más subconjuntos de la población pediátrica con diabetes mellitus tipo 2 (ver sección 4.2 para obtener información sobre uso pediátrico).
05.2 "Propiedades farmacocinéticas -
Las características de absorción de exenatida reflejan las características de liberación sostenida de la formulación de liberación sostenida de exenatida. Una vez absorbida en la circulación, la exenatida se distribuye y elimina de acuerdo con las propiedades farmacocinéticas sistémicas conocidas (como se describe en esta sección).
Absorción
Después de la administración semanal de 2 mg de exenatida de liberación prolongada, las concentraciones medias de exenatida excedieron las concentraciones mínimas efectivas (~ 50 pg / ml) en 2 semanas con un aumento gradual de la concentración plasmática media de exenatida durante 6-7 semanas. Concentraciones de exenatida de aproximadamente 300 pg / ml. mL se mantuvieron indicando que se ha alcanzado el estado estacionario. Las concentraciones en estado estacionario de exenatida se mantienen durante el intervalo de tiempo de una semana entre dosis con una fluctuación mínima (de picos y valles) a partir de esta concentración terapéutica media.
Distribución
El volumen medio aparente de distribución de exenatida tras la administración subcutánea de una dosis única de exenatida es de 28 L.
Biotransformación y eliminación
Los estudios no clínicos han demostrado que la exenatida se elimina principalmente por filtración glomerular con degradación proteolítica posterior. El aclaramiento aparente medio de exenatida es de 9 l / h. Estas características farmacocinéticas de exenatida son independientes de la dosis. Aproximadamente 10 semanas después de la interrupción del tratamiento con exenatida de liberación prolongada, las concentraciones plasmáticas de exenatida cayeron por debajo de las concentraciones mínimas detectables.
Poblaciones especiales
Daño en el riñón
El análisis farmacocinético poblacional de pacientes con insuficiencia renal que recibieron 2 mg de exenatida de liberación prolongada indica que puede haber un aumento en la exposición sistémica de aproximadamente 74% y 23% (mediana de predicción en cada grupo), respectivamente. En pacientes con moderada (N = 10) y insuficiencia renal leve (N = 56) en comparación con pacientes con función renal normal (N = 84).
Insuficiencia hepática
No se han realizado estudios farmacocinéticos en pacientes con insuficiencia hepática. La exenatida se elimina principalmente por vía renal; por lo tanto, no se espera que la disfunción hepática altere las concentraciones plasmáticas de exenatida.
Sexo, raza y peso corporal
El sexo, la raza y el peso corporal no tienen una influencia clínicamente relevante sobre las propiedades farmacocinéticas de exenatida.
Personas mayores
Los datos en pacientes de edad avanzada son limitados, pero no sugieren cambios marcados en la exposición a exenatida con el aumento de la edad hasta aproximadamente 75 años.
En un estudio farmacocinético de exenatida de liberación inmediata en pacientes con diabetes tipo 2, la administración de exenatida (10 microgramos) dio como resultado un aumento medio del AUC de exenatida del 36% en 15 sujetos de edad avanzada de 75 a 85 años en comparación con 15 sujetos de 45 años de edad. y 65 años probablemente relacionados con una función renal reducida en el grupo de mayor edad (ver sección 4.2).
Población pediátrica
En un estudio farmacocinético con exenatida de liberación inmediata en 13 pacientes con diabetes tipo 2 de 12 a 16 años de edad, la administración de exenatida (5 microgramos) como dosis única dio como resultado valores medios de AUC (16% inferiores) y Cmax ( 25% menos) que los observados en pacientes adultos No se han realizado estudios farmacocinéticos con exenatida de liberación prolongada en la población pediátrica.
05.3 Datos preclínicos sobre seguridad -
Los datos de los estudios no clínicos no muestran riesgos especiales para los seres humanos según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas o genotoxicidad realizados con exenatida de liberación inmediata o de liberación prolongada.
En un estudio de carcinogenicidad de 104 semanas con exenatida de liberación prolongada, se observó un aumento estadísticamente significativo en la incidencia de tumores de células C de tiroides (adenoma y / o carcinoma) en ratas a todas las dosis (1,4 a 26 veces la exposición clínica en humanos). con exenatida de liberación prolongada) Actualmente se desconoce la relevancia de estos hallazgos para los seres humanos.
Los estudios en animales con exenatida no indicaron efectos nocivos directos sobre la fertilidad; altas dosis de exenatida causaron efectos sobre el esqueleto y redujeron el desarrollo fetal y neonatal.
06.0 INFORMACIÓN FARMACÉUTICA -
06.1 Excipientes -
Polvo
poli (D, L-lactida-co-glicólido);
sacarosa.
Solvente
croscarmelosa sódica;
cloruro de sodio;
polisorbato 20;
dihidrogenofosfato de sodio monohidrato;
fosfato disódico heptahidratado;
agua para preparaciones inyectables.
06.2 Incompatibilidad "-
En ausencia de estudios de compatibilidad, este medicamento no debe mezclarse con otros medicamentos.
06.3 Período de validez "-
3 años.
Después de la suspensión
La suspensión debe inyectarse inmediatamente después de mezclar el polvo y el disolvente.
06.4 Precauciones especiales de conservación
Conservar en nevera (entre 2 ° C y 8 ° C).
No congelar.
Antes de su uso, el kit se puede conservar hasta 4 semanas a una temperatura inferior a 30 ° C.
Conservar en el paquete original para proteger el medicamento de la luz.
Para conocer las condiciones de almacenamiento después de mezclar el medicamento, ver sección 6.3.
06.5 Naturaleza del envase primario y contenido del envase.
El polvo se envasa en un vial de vidrio tipo I de 3 ml cerrado con un disco de goma de clorobutilo y un sello de aluminio con una tapa de plástico flip-off.
El disolvente se envasa en una jeringa precargada de vidrio de tipo I de 1,5 ml cerrada con un tapón de goma de bromobutilo y un émbolo de goma.
Cada kit monodosis contiene un vial con 2 mg de exenatida, una jeringa precargada con 0,65 ml de disolvente, un conector para el vial y dos agujas de inyección (una de repuesto).
Envase de 4 kits monodosis y envase múltiple que contiene 12 kits monodosis (3 envases x 4). Es posible que no se comercialicen todos los tamaños de envases.
06.6 Instrucciones de uso y manipulación -
Se debe advertir al paciente que deseche la aguja de forma segura, con la aguja aún insertada después de cada inyección. El paciente no necesita conservar ningún componente del kit desechable.
El solvente debe ser inspeccionado visualmente antes de su uso. El solvente solo debe usarse si es transparente y no tiene partículas. Después de la suspensión, la mezcla solo debe usarse si tiene un aspecto de blanco a blanquecino y turbio.
La exenatida de liberación prolongada debe inyectarse inmediatamente después de la suspensión del polvo en el disolvente.
No se debe usar exenatida de liberación prolongada si se ha congelado.
Los medicamentos no utilizados y los desechos derivados de este medicamento deben eliminarse de acuerdo con las regulaciones locales.
07.0 TITULAR DE LA "AUTORIZACIÓN DE COMERCIALIZACIÓN" -
AstraZeneca AB
SE-151 85 Södertälje
Suecia
08.0 NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN -
EU / 1/11/696 / 001-002
041276015
041276027
09.0 FECHA DE LA PRIMERA AUTORIZACIÓN O RENOVACIÓN DE LA AUTORIZACIÓN -
Fecha de la primera autorización: 17 de junio de 2011
Fecha de la renovación más reciente: 17 de junio de 2016
10.0 FECHA DE REVISIÓN DEL TEXTO -
Febrero de 2016