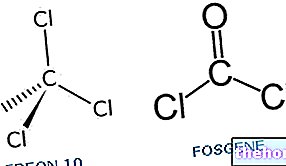
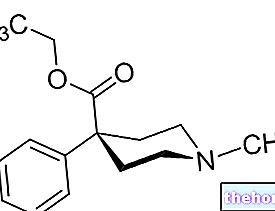
de calcio y ácidos inorgánicos, como por ejemplo ácido nítrico, ácido clorhídrico o ácido sulfúrico. A continuación se muestra la reacción química que implica el uso de este último ácido:
Ca3 (PO4) 2 + 3 H2SO4 → 3 CaSO4 + 2 H3PO4
El proceso térmico, en cambio, implica la obtención de anhídrido fosfórico a partir del fósforo elemental. Una vez formado, el anhídrido debe hidratarse hasta obtener el ácido ortofosfórico, como se ilustra en la siguiente reacción:
P2O5 + 3 H2O → 2 H3PO4
Este último proceso generalmente da lugar a un ácido ortofosfórico más puro que el proceso húmedo.
ambiental, aparece como un sólido blanco que se derrite a una temperatura de aproximadamente 42 ° C.
Sin embargo, el ácido fosfórico se comercializa generalmente en forma de una solución acuosa concentrada al 85%. Es una solución incolora, inodoro y no volátil, pero corrosiva y con una consistencia bastante densa, casi "almibarada".
Además de ser soluble en agua, el ácido ortofosfórico también es soluble en etanol. No es ni explosivo ni inflamable, pero debido a su corrosividad para la piel y las membranas mucosas, debe manejarse con mucho cuidado.
para favorecer la adhesión de materiales de cementación para cápsulas, puentes, carillas, empastes, etc. En este contexto, el ácido ortofosfórico se utiliza generalmente en soluciones al 37%.
-cos-dove-si-trova-e-tossicit.jpg)