Editado por el Dr. Giovanni Chetta
La ECM se describe generalmente como compuesta de varias clases grandes de biomoléculas:
- Proteínas estructurales (colágeno y elastina)
- Proteínas especializadas (fibrilina, fibronectina, laminina, etc.)
- Proteoglicanos (agrecanos, sindecanos) y glusaminoglicanos (hialuronanos, condroitín sulfatos, heparán sulfatos, etc.)
Proteínas estructurales
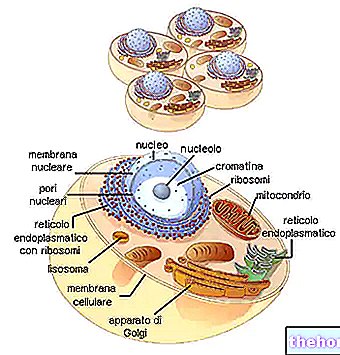
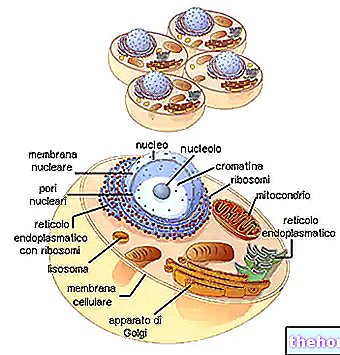
Los colágenos forman la familia de glicoproteínas más representada en el reino animal. Son las proteínas más presentes en la matriz extracelular (pero no las más importantes) y son los constituyentes fundamentales de los tejidos conectivos propiamente dichos (cartílago, hueso, fascia, tendones, ligamentos).
Existen al menos 16 tipos diferentes de colágeno, de los cuales los tipos I, II y III son los más presentes a nivel de las fibrillas típicas (el tipo IV forma una especie de retículo que representa el componente mayoritario de las láminas basales).
Los colágenos son principalmente sintetizados por fibroblastos, pero las células epiteliales también pueden sintetizarlos.
Las fibras de colágeno interactúan continuamente con una enorme cantidad de otras moléculas de la matriz extracelular, constituyendo un continuo biológico fundamental para la vida de la célula. Los colágenos asociados en las fibrillas juegan un papel predominante en la formación y mantenimiento de estructuras capaces de resistir las fuerzas de tensión. siendo casi inelástica (los glucosamlicanos realizan una acción de resistencia a la compresión). De alguna manera el colágeno se produce y re-metaboliza en función de la carga mecánica y sus propiedades viscoelásticas conllevan, como veremos en el párrafo "Viscoelasticidad de la fascia ", un gran impacto en la postura del hombre. Como demostración adicional de la capacidad del colágeno para cambiar de acuerdo con las influencias ambientales, asumiendo, por ejemplo,. grados variables de rigidez, elasticidad y resistencia, existen colágenos, definidos con el término FACIT (colágeno asociado a fibrillas con triple hélices interrumpidas) capaces de funcionar funcionalmente como proteoglicanos (descritos en el párrafo "Glucosaminoglicanos y proteoglicanos").
Las fibras de colágeno, gracias a su recubrimiento de PG / GAG (proteoglicanos / glucosaminoglicanos) poseen propiedades de biosensores y bioconductores: las cargas eléctricas relativas dan como resultado una mayor capacidad para unir agua e intercambiar iones, por lo tanto, una mayor capacidad eléctrica.
Sabemos que cualquier fuerza mecánica capaz de generar una deformación estructural tensiona los enlaces intermoleculares, produciendo un ligero flujo eléctrico, que es el corriente piezoeléctrica (Athenstaedt, 1969). En tales casos, las fibras de colágeno distribuyen las cargas positivas en su superficie convexa y las negativas en la cóncava, transformándose así en semiconductores (permiten el flujo de electrones en su superficie unidireccional). Dado que la energía piezoeléctrica (así como la energía piroeléctrica generada por tensiones térmicas) es neutralizada por los iones circulantes en muy poco tiempo (aproximadamente 10-7 - 10-9 segundos), la disposición del PG / GAG en la señal es decisivo para la propagación de la señal.superficie de las fibrillas, como para actuar como "repetidores" del impulso eléctrico. En particular, una periodicidad longitudinal de aprox. 64 nm (que bajo el microscopio óptico aparece como una raya) permite una velocidad de propagación del impulso igual a aproximadamente 64 m / s (correspondiente a la velocidad de conducción de las fibras nerviosas rápidas) - Rengling, 2001. El fuerte momento dipolar de las fibrillas de colágeno y su capacidad de resonancia (propiedad común a todas las estructuras peptídicas), así como la baja constante dieléctrica del MEC, facilitan la transmisión de señales electromagnéticas. Por tanto, la red de colágeno tridimensional y ubicua también posee la peculiar característica de conducir señales bioeléctricas en las tres dimensiones del espacio, basadas en la disposición relativa entre las fibrillas de colágeno y las células, en la dirección aferente (de la ECM a las células) o, viceversa, eferente.
Todo esto representa un sistema de comunicación de células MEC en tiempo real y tales bio-señales electromagnéticas pueden conducir a cambios bioquímicos importantes, por ejemplo, en el hueso, los osteoclastos no pueden "digerir" el hueso cargado piezoeléctricamente (Oschman, 2000).
Por último, cabe destacar que la célula, como era de esperar, produce de forma continua y con un gasto energético considerable (aprox. 70%) material que necesariamente debe ser expulsado, mayoritariamente a través del almacenamiento exclusivo de protocolágeno (precursor biológico del colágeno) en determinadas vesículas (Albergati, 2004).
La gran mayoría de los tejidos de los vertebrados requieren la presencia simultánea de dos características vitales: fuerza y elasticidad. Una verdadera red de fibras elásticas, ubicada en el interior de la ECM de estos tejidos, permite volver a las condiciones iniciales después de fuertes tracciones, las fibras elásticas son capaces de aumentar la extensibilidad de un órgano o de una parte de él al menos cinco veces. Las fibras de colágeno largas e inelásticas se intercalan entre las fibras elásticas con la tarea precisa de limitar la "deformación excesiva debido a la tracción de los tejidos. L"elastina representa el componente principal de las fibras elásticas. Es una proteína extremadamente hidrófoba, de unos 750 aminoácidos de longitud, ya que el colágeno es rico en prolina y glicina pero, a diferencia del colágeno, no está glucosilada y contiene muchos residuos de hidroxiprolina y no hidroxilisina. La elastina aparece como una verdadera red bioquímica de forma irregularmente tridimensional, compuesta por fibras y laminillas que impregnan la ECM de todos los tejidos conectivos. Se encuentra en cantidades particularmente abundantes en los vasos sanguíneos con características elásticas (es la proteína de la ECM más presente en las arterias y representa más del 50% del peso seco total de la aorta), en los ligamentos, en el pulmón y en la piel. En la dermis, al contrario de lo que ocurre con el colágeno, la densidad y el volumen de la elastina tienden a aumentar con el tiempo, pero la elastina vieja generalmente aparece hinchada, casi hinchada, a menudo con un aspecto fragmentado y con una reducción del componente "amorfo". (Pasquali Rochetti et al, 2004). Las células del músculo liso y los fibroblastos son los principales productores de su precursor, la tropoelastina, secretada en los espacios extracelulares.
Otros artículos sobre "Colágeno y elastina, fibras de colágeno en la matriz extracelular"
- La matriz extracelular
- Fibronectina, glucosaminoglicanos y proteoglicanos
- Importancia de la matriz extracelular en los equilibrios celulares
- Alteraciones de la matriz extracelular y patologías
- Tejido conectivo y matriz extracelular
- Fascia profunda: tejido conectivo
- Mecanorreceptores fasciales y miofibroblastos
- Biomecánica profunda de la fascia
- Postura y equilibrio dinámico
- Tensegridad y movimientos helicoidales
- Extremidades inferiores y movimiento corporal.
- Soporte de nalgas y aparato estomatognático
- Casos clínicos, alteraciones posturales
- Casos clínicos, postura
- Evaluación postural - Caso clínico
- Bibliografía: de la matriz extracelular a la postura. ¿Es el sistema conectivo nuestro verdadero Deus ex machina?