¿Qué es Luveris?
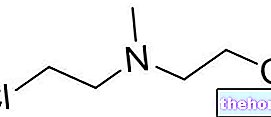
Luveris es un medicamento que contiene el principio activo lutropina alfa. Está disponible como polvo y disolvente para preparar una solución inyectable y como solución inyectable en un cartucho.
¿Para qué se utiliza Luveris?
Luveris se utiliza en el tratamiento de la infertilidad y, junto con la hormona estimulante del folículo (FSH), estimula la maduración de los óvulos en los ovarios de mujeres con deficiencia grave (niveles muy bajos) de hormona luteinizante (LH) y FSH.
La medicina solo se puede obtener con una receta.
¿Cómo se usa Luveris?
El tratamiento con Luveris debe ser realizado por médicos con experiencia en el tratamiento de la infertilidad.
Luveris se administra junto con FSH una vez al día. Se debe controlar la respuesta al tratamiento para controlar la evolución del desarrollo del óvulo en el ovario. La dosis de FSH debe ajustarse según la respuesta de la paciente y el tratamiento puede durar hasta cinco semanas. Luveris se administra mediante una inyección debajo de la piel (debajo de la piel). La inyección puede ser practicada por la propia paciente debidamente instruida por el médico y con la condición de que tenga la posibilidad de consultar con un experto.
Si se utilizan el polvo y el disolvente, deben mezclarse inmediatamente antes de su uso. La solución resultante se puede mezclar con FSH en la misma jeringa. Un vial de polvo y disolvente son para un solo uso, pero cada cartucho de solución contiene seis dosis de Luveris.
¿Cómo actúa Luveris?
El principio activo de Luveris es lutropina alfa, una réplica de la hormona LH producida naturalmente. Cuando se libera en el organismo, la hormona LH hace que los óvulos se liberen (ovulación) durante el ciclo menstrual.Luveris se usa en combinación con FSH, que también estimula la ovulación.
La lutropina alfa se produce mediante un método denominado «tecnología del ADN recombinante»: la fabrica una célula que ha recibido un gen (ADN) que la hace capaz de producir LH humana.
¿Qué tipo de estudios se han realizado con Luveris?
Luveris, administrado con FSH, fue objeto de un estudio principal en el que participaron 38 mujeres con deficiencia grave de LH y FSH. Debido al pequeño número de pacientes con esta disfunción, Luveris no se comparó con ningún otro medicamento. La principal medida de eficacia fue la cantidad de mujeres que produjeron folículos funcionales (óvulos dentro de los ovarios listos para ser liberados).
¿Qué beneficio ha demostrado tener Luveris durante los estudios?
En el estudio principal, el 67% de las mujeres que tomaron la dosis aprobada de Luveris (75 unidades internacionales) en combinación con FSH produjeron folículos funcionales (6 de 9). Las dosis más altas no mostraron mayor eficacia que con esta dosis.
¿Cuál es el riesgo asociado a Luveris?
Los efectos secundarios más comunes observados con Luveris (observados en 1 a 10 pacientes de cada 100) son reacciones en el lugar de la inyección, dolor de cabeza, somnolencia, náuseas, dolor abdominal, dolor en la región pélvica (parte inferior del abdomen), síndrome de hiperestimulación ovárica (como náuseas, aumento de peso y diarrea), quistes ováricos (desarrollo de una cavidad llena de líquido en los ovarios) y dolor en las mamas.El síndrome de hiperestimulación ovárica ocurre cuando los ovarios responden en exceso al tratamiento, especialmente si se han utilizado medicamentos para estimular la ovulación. Para obtener la lista completa de efectos secundarios notificados con Luveris, consulte el prospecto.
Luveris no debe administrarse a personas que puedan ser hipersensibles (alérgicas) a "LH", FSH u otros componentes del medicamento. No debe usarse en mujeres con cáncer de glándula pituitaria, hipotálamo, mama, útero u ovarios. Tampoco debe usarse en presencia de agrandamiento de los ovarios o la presencia de quistes no debidos a una enfermedad de ovario poliquístico, o sangrado vaginal inexplicable Para la lista completa de restricciones de uso, consulte el prospecto.
¿Por qué se ha aprobado Luveris?
El Comité de Medicamentos de Uso Humano (CHMP) decidió que los beneficios de Luveris son mayores que sus riesgos en combinación con una preparación de FSH para estimular el desarrollo folicular en mujeres con deficiencia grave de LH y FSH. El comité recomendó la concesión de una autorización de comercialización para Luveris.
Otras informaciones sobre Luveris:
El 29 de noviembre de 2000, la Comisión Europea otorgó a Serono Europe Limited una "Autorización de comercialización" para Luveris, válida en toda la Unión Europea. La "Autorización de comercialización" fue renovada el 29 de noviembre de 2005.
Para obtener la versión completa del EPAR de Luveris, haga clic aquí.
Última actualización de este resumen: 04-2009.
La información sobre Luveris - Lutropin alfa publicada en esta página puede estar desactualizada o incompleta. Para un uso correcto de esta información, consulte la página de exención de responsabilidad e información útil.