Ingredientes activos: Etonogestrel / Etinilestradiol
NuvaRing, 0,120 mg / 0,015 mg cada 24 horas, dispositivo vaginal
¿Por qué se usa Nuvaring? ¿Para qué sirve?
NuvaRing es un anillo vaginal anticonceptivo que se usa para prevenir el embarazo. Cada anillo contiene una pequeña cantidad de dos hormonas sexuales femeninas: etonogestrel y etinilestradiol. El anillo libera estas hormonas lentamente en el torrente sanguíneo. Debido a que las cantidades de hormonas liberadas son bajas, NuvaRing se considera un anticonceptivo hormonal de dosis baja. Dado que NuvaRing libera dos tipos diferentes de hormonas, es un anticonceptivo hormonal combinado.
NuvaRing funciona como una píldora anticonceptiva combinada (la píldora), pero en lugar de tomar una píldora todos los días, el anillo se usa durante tres semanas seguidas. NuvaRing libera dos hormonas sexuales femeninas que impiden la liberación de un óvulo de los ovarios. no hay liberación de óvulos, no es posible quedar embarazada.
Contraindicaciones cuando no se debe usar Nuvaring
Notas generales Antes de comenzar a usar NuvaRing, debe leer la información sobre coágulos de sangre. Es especialmente importante que lea los síntomas de un coágulo de sangre.
Este prospecto describe algunas situaciones en las que el uso de NuvaRing debe suspenderse o NuvaRing puede ser menos confiable. En tales situaciones, no debe tener relaciones sexuales o debe tomar precauciones anticonceptivas no hormonales adicionales, como el uso de condón u otro método de barrera. . No utilice métodos de ritmo y temperatura basal, que pueden ser poco fiables, ya que NuvaRing altera los cambios mensuales en la temperatura corporal y el moco cervical.
NuvaRing, al igual que otros anticonceptivos hormonales, no protege contra la infección por VIH (SIDA) o cualquier otra enfermedad de transmisión sexual.
No use NuvaRing si tiene alguna de las condiciones que se enumeran a continuación. Si tiene alguna de las afecciones que se enumeran a continuación, comuníquese con su médico. Su médico discutirá con usted otros métodos anticonceptivos que pueden ser más adecuados para usted.
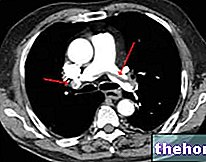
- si tiene (o ha tenido alguna vez) un coágulo de sangre en un vaso sanguíneo de la pierna (trombosis venosa profunda, TVP), pulmón (embolia pulmonar, EP) u otros órganos; 2 54 mm 4 mm
- si sabe que tiene un trastorno que afecta la coagulación de la sangre, como deficiencia de proteína C, deficiencia de proteína S, deficiencia de antitrombina III, factor V Leiden o anticuerpos antifosfolípidos;
- si va a someterse a una "operación o si va a permanecer acostado durante mucho tiempo (ver sección" Coágulos de sangre ");
- si alguna vez ha tenido un ataque al corazón o un derrame cerebral;
- si tiene (o ha tenido alguna vez) angina de pecho (una afección que causa dolor de pecho intenso y puede ser el primer signo de un ataque cardíaco) o un ataque isquémico transitorio (AIT - síntomas temporales de accidente cerebrovascular);
si padece alguna de las siguientes enfermedades, que podrían aumentar el riesgo de formación de coágulos de sangre en las arterias:
- diabetes grave con lesión de los vasos sanguíneos
- presión arterial muy alta
- nivel muy alto de grasas (colesterol o triglicéridos) en la sangre
- una enfermedad conocida como hiperhomocisteinemia
no use Nuvaring
- si tiene (o ha tenido alguna vez) un tipo de migraña llamada "migraña con aura";
- si tiene (o ha tenido alguna vez) inflamación del páncreas (pancreatitis) asociada con niveles altos de grasa en sangre.
- si tiene (o ha tenido alguna vez) una enfermedad hepática grave y su función hepática aún no ha vuelto a la normalidad.
- si tiene (o ha tenido alguna vez) un tumor de hígado benigno o maligno.
- si tiene (o ha tenido alguna vez) o puede tener cáncer de mama o de órganos genitales.
- si tiene sangrado vaginal de origen desconocido.
- si es alérgico al etinilestradiol o al etonogestrel oa cualquiera de los demás componentes de este medicamento
Si alguna de estas condiciones aparece por primera vez mientras usa el NuvaRing, quítese inmediatamente el anillo y consulte a su médico. Mientras tanto, utilice métodos anticonceptivos no hormonales.
Precauciones de uso Lo que necesita saber antes de tomar Nuvaring
¿Cuándo debería consultar a un médico?
Comuníquese con un médico urgentemente
- si nota posibles signos de un coágulo de sangre que pueden indicar que padece un coágulo de sangre en la pierna (trombosis venosa profunda), un coágulo de sangre en el pulmón (embolia pulmonar), un ataque cardíaco o un ictus (ver sección siguiente). "Coágulos de sangre").
Para obtener una descripción de los síntomas de estos efectos secundarios graves, consulte la sección "Cómo reconocer un coágulo de sangre".
Informe a su médico si se encuentra en alguna de las situaciones siguientes. Si esta afección aparece o empeora mientras está usando NuvaRing, debe informar a su médico.
- si un familiar cercano tiene o ha tenido cáncer de mama;
- si tiene epilepsia (ver sección "Interacciones");
- si tiene una enfermedad del hígado (p. ej., ictericia) o enfermedad de la vesícula biliar (p. ej., cálculos biliares);
- si tiene enfermedad de Crohn o colitis ulcerosa (enfermedad intestinal inflamatoria crónica);
- si tiene lupus eritematoso sistémico (LES, una enfermedad que afecta al sistema de defensa natural);
- si tiene síndrome urémico hemolítico (SUH, un trastorno de la coagulación de la sangre que causa insuficiencia renal);
- si tiene anemia de células falciformes (una enfermedad hereditaria de los glóbulos rojos);
- si tiene niveles altos de grasa en la sangre (hipertrigliceridemia) o "antecedentes familiares positivos de esta afección". La hipertrigliceridemia se ha asociado con un mayor riesgo de desarrollar pancreatitis (inflamación del páncreas);
- si va a someterse a una "operación o si va a permanecer acostado durante mucho tiempo (ver sección" Coágulos de sangre ");
- si acaba de dar a luz, su riesgo de desarrollar coágulos de sangre es mayor. Pregúntele a su médico cuándo puede comenzar a usar NuvaRing después de dar a luz;
- si tiene "inflamación de las venas debajo de la piel (tromboflebitis superficial);
- si tiene varices;
- si tiene una afección que se presentó por primera vez, o que empeoró, durante el embarazo o durante el uso previo de hormonas sexuales (por ejemplo, pérdida de audición, porfiria [un trastorno de la sangre], herpes gestacional [erupción cutánea] con ampollas durante el embarazo], enfermedad de Sydenham corea [una enfermedad de los nervios en la que pueden ocurrir movimientos corporales repentinos], angioedema hereditario [debe consultar a su médico inmediatamente si experimenta síntomas de angioedema, como hinchazón de la cara, lengua y / o garganta y / o dificultad para tragar o urticaria asociada con dificultad para respirar]).
- si tiene (o ha tenido alguna vez) cloasma (manchas de pigmentación de color marrón amarillento, las llamadas `` manchas del embarazo '', especialmente en la cara). Si es así, evite la exposición prolongada al sol o los rayos ultravioleta.
- si padece una afección médica que dificulta el uso de NuvaRing, como estreñimiento, prolapso cervical o dolor durante las relaciones sexuales.
COÁGULOS DE SANGRE
El uso de un anticonceptivo hormonal combinado como NuvaRing aumenta el riesgo de desarrollar un coágulo de sangre en comparación con no usarlo. En casos raros, un coágulo de sangre puede bloquear los vasos sanguíneos y causar problemas graves. Pueden desarrollarse coágulos de sangre.
en las venas (llamado "trombosis venosa", "tromboembolismo venoso" o TEV)
en las arterias (denominado "trombosis arterial", "tromboembolismo arterial" o ATE).
La recuperación de los coágulos de sangre no siempre es completa. En raras ocasiones, pueden producirse efectos graves duraderos o, muy raramente, pueden ser mortales.
Es importante recordar que el riesgo general de un coágulo sanguíneo dañino asociado con NuvaRing es bajo.
CÓMO RECONOCER UN COÁGULO DE SANGRE
Consulte a un médico de inmediato si nota alguno de los siguientes signos o síntomas.
- hinchazón de una pierna oa lo largo de una vena de la pierna o el pie, especialmente cuando se acompaña de:
- dolor o sensibilidad en la pierna que solo se puede sentir al pararse o caminar
- aumento de la sensación de calor en la pierna afectada
- cambio de color de la piel de la pierna, como palidez, rojo o azul
- dificultad para respirar repentina e inexplicable o respiración rápida;
- tos repentina sin una causa obvia, que posiblemente cause la emisión de sangre;
- dolor agudo en el pecho que puede aumentar con la respiración profunda;
- aturdimiento o mareo severo;
- latidos cardíacos rápidos o irregulares;
- dolor severo en el estómago
- pérdida inmediata de la visión o
- Visión borrosa indolora que puede progresar a pérdida de la visión.
- dolor, malestar, sensación de presión o pesadez en el pecho
- sensación de opresión o plenitud en el pecho, brazo o debajo del esternón;
- sensación de plenitud, indigestión o asfixia;
- malestar de la parte superior del cuerpo que se irradia a la espalda, la mandíbula, la garganta, los brazos y el estómago;
- sudoración, náuseas, vómitos o mareos;
- debilidad extrema, ansiedad o dificultad para respirar;
- latidos cardíacos rápidos o irregulares
- entumecimiento o debilidad repentinos de la cara, brazo o pierna, especialmente en un lado del cuerpo;
- confusión repentina, dificultad para hablar o comprender;
- dificultad repentina para ver con uno o ambos ojos;
- dificultad repentina para caminar, mareos, pérdida del equilibrio o la coordinación;
- migraña repentina, intensa o prolongada sin causa conocida;
- pérdida del conocimiento o desmayos con o sin convulsiones.
- hinchazón y decoloración azul pálido de una "extremidad;
- dolor de estómago severo (abdomen agudo).
COÁGULOS DE SANGRE EN UNA VENA
¿Qué puede suceder si se forma un coágulo de sangre en una vena?
- El uso de anticonceptivos hormonales combinados se ha relacionado con un mayor riesgo de formación de coágulos de sangre en las venas (trombosis venosa). Sin embargo, estos efectos secundarios son raros. En la mayoría de los casos, ocurren durante el primer año de uso de un anticonceptivo hormonal combinado.
- Si se forma un coágulo de sangre en una vena de la pierna o el pie, puede causar una trombosis venosa profunda (TVP).
- Si un coágulo de sangre sale de la pierna y se aloja en el pulmón, puede provocar una "embolia pulmonar".
- En muy raras ocasiones, se puede formar un coágulo en otro órgano como el ojo (trombosis de las venas retinianas).
¿Cuándo es mayor el riesgo de desarrollar un coágulo de sangre en una vena?
El riesgo de desarrollar un coágulo de sangre en una vena es mayor durante el primer año de tomar un anticonceptivo hormonal combinado por primera vez. El riesgo puede ser aún mayor si vuelve a tomar un anticonceptivo hormonal combinado (el mismo medicamento o un medicamento diferente) después de un descanso de 4 semanas o más.
Después del primer año, el riesgo se reduce pero siempre es ligeramente más alto que si no estuviera usando un anticonceptivo hormonal combinado.
Cuando deja de tomar NuvaRing, su riesgo de desarrollar un coágulo sanguíneo vuelve a la normalidad en unas pocas semanas.
¿Cuál es el riesgo de desarrollar un coágulo de sangre?
El riesgo depende de su riesgo natural de TEV y del tipo de anticonceptivo hormonal combinado que esté tomando.
El riesgo general de desarrollar un coágulo de sangre en la pierna o el pulmón (TVP o EP) con NuvaRing es bajo.
- De cada 10,000 mujeres que no están usando ningún anticonceptivo hormonal combinado y que no están embarazadas, aproximadamente 2 desarrollarán un coágulo de sangre en un año.
- De cada 10,000 mujeres que están usando un anticonceptivo hormonal combinado que contiene levonorgestrel, noretisterona o norgestimato, alrededor de 5-7 desarrollarán un coágulo de sangre en un año.
- De cada 10.000 mujeres que están usando un anticonceptivo hormonal combinado que contiene norelgestromina o etonorgestrel como NuvaRing, alrededor de 6-12 desarrollarán un coágulo de sangre en un año.
- El riesgo de que se forme un coágulo de sangre depende de su historial médico (consulte "Factores que aumentan el riesgo de que se forme un coágulo de sangre").
Factores que aumentan el riesgo de desarrollar un coágulo de sangre en una vena.
El riesgo de desarrollar un coágulo de sangre con NuvaRing es bajo, pero algunas afecciones aumentan el riesgo. Su riesgo es mayor:
- si tiene un sobrepeso grave (índice de masa corporal o IMC superior a 30 kg / m2);
- si un pariente cercano ha tenido un coágulo de sangre en la pierna, pulmón u otro órgano a una edad temprana (menos de 50 años aproximadamente). En este caso, podría tener un trastorno hereditario de la coagulación de la sangre;
- si va a someterse a una operación o si tiene que permanecer acostado durante mucho tiempo debido a una lesión o enfermedad o si tiene una pierna escayolada, es posible que deba dejar de tomar NuvaRing unas semanas antes de la cirugía o en período en el que tiene menos movilidad Si tiene que dejar de tomar NuvaRing, pregunte a su médico cuándo puede empezar a tomarlo de nuevo;
- a medida que envejece (especialmente a partir de los 35 años);
- si dio a luz hace menos de unas semanas.
El riesgo de desarrollar un coágulo de sangre aumenta cuantas más afecciones tenga de este tipo.
Los viajes en avión (que duran> 4 horas) pueden aumentar temporalmente el riesgo de un coágulo de sangre, especialmente si tiene algunos de los otros factores de riesgo enumerados.
Es importante que informe a su médico si se encuentra en alguna de estas situaciones, incluso si no está seguro. Su médico puede decidir que deje de tomar NuvaRing Si alguna de las condiciones anteriores cambia mientras está usando NuvaRing, por ejemplo, si un pariente cercano tiene una trombosis sin un motivo conocido o si usted aumenta mucho de peso, comuníquese con su médico.
COÁGULOS DE SANGRE EN UNA ARTERIA
¿Qué puede suceder si se forma un coágulo de sangre en una "arteria"?
Al igual que los coágulos de sangre en una vena, los coágulos en una arteria pueden causar problemas graves, por ejemplo, pueden causar un ataque cardíaco o un derrame cerebral.
Factores que aumentan el riesgo de desarrollar un coágulo de sangre en una arteria
Es importante tener en cuenta que el riesgo de ataque cardíaco o accidente cerebrovascular asociado con el uso de NuvaRing es muy bajo pero puede aumentar:
- con el aumento de la edad (más de 35 años);
- si fuma. Cuando utilice un anticonceptivo hormonal combinado como NuvaRing, se le aconseja que deje de fumar. Si no puede dejar de fumar y tiene más de 35 años, su médico puede recomendarle que utilice un tipo diferente de anticonceptivo;
- si tiene sobrepeso;
- si tiene la presión arterial alta;
- si un miembro de su familia inmediata ha tenido un ataque cardíaco o un derrame cerebral a una edad temprana (menos de 50 años aproximadamente). En este caso, también puede tener un alto riesgo de sufrir un ataque cardíaco o un derrame cerebral;
- si usted o un familiar cercano tiene un nivel elevado de grasas en sangre (colesterol o triglicéridos);
- si padece migrañas, especialmente migrañas con aura;
- si tiene algún problema cardíaco (defecto de la válvula, un trastorno del ritmo cardíaco llamado fibrilación auricular);
- si tiene diabetes.
Si tiene más de una de estas afecciones, o si alguna de ellas es particularmente grave, el riesgo de desarrollar un coágulo de sangre puede ser aún mayor.
Si alguna de las afecciones anteriores cambia mientras está usando NuvaRing, por ejemplo, si comienza a fumar, si un pariente cercano tiene una trombosis sin una razón conocida o si aumenta mucho de peso, comuníquese con su médico.
Tumores
La siguiente información se obtuvo en estudios de COC y también se puede aplicar al NuvaRing.
No hay información disponible sobre la administración vaginal de hormonas anticonceptivas (como NuvaRing). Los diagnósticos de cáncer de mama son un poco más comunes en mujeres que usan la píldora combinada, pero no se sabe si esto es causado por el tratamiento. Por ejemplo, puede ser que los cánceres se encuentren más en mujeres que toman la píldora combinada porque su médico las revisa con más frecuencia.El aumento en la aparición de cáncer de mama disminuye gradualmente después de suspender la píldora combinada.
Es importante examinarse las mamas con regularidad y ponerse en contacto con su médico tan pronto como sienta un bulto. También debe informar a su médico si un pariente cercano tiene o alguna vez ha tenido cáncer de mama (ver sección 2.2 "Advertencias y precauciones').
Rara vez se han informado tumores hepáticos benignos y, en pocos casos, aún tumores hepáticos malignos en mujeres que toman la píldora anticonceptiva. Consulte a su médico en caso de dolor severo inusual en el abdomen.
En mujeres que usan la píldora combinada, se ha informado que el cáncer de endometrio (el revestimiento del útero) y el cáncer de ovarios ocurren con menos frecuencia. Este también puede ser el caso de NuvaRing, pero no se ha confirmado.
Interacciones ¿Qué medicamentos o alimentos pueden cambiar el efecto de Nuvaring?
Informe siempre al médico que le prescribe NuvaRing sobre cualquier medicamento o producto a base de hierbas que ya esté tomando, y también informe a cualquier otro médico o dentista (o farmacéutico dispensador) que le receten otros medicamentos que está usando NuvaRing, para que puedan determinar si y cómo durante mucho tiempo es necesario utilizar métodos anticonceptivos adicionales.
Algunos medicamentos pueden causar problemas especiales cuando se usan anticonceptivos hormonales, como NuvaRing.
Existen medicamentos que pueden provocar una disminución de la eficacia anticonceptiva de NuvaRing o causar hemorragias inesperadas. Estos incluyen los que se utilizan para tratar:
- l "epilepsia (por ejemplo, primidona, fenitoína, barbitúricos, carbamazepina, oxcarbazepina, topiramato, felbamato);
- tuberculosis (por ejemplo, rifampicina);
- Infección por VIH (por ejemplo, ritonavir);
- otras enfermedades infecciosas (por ejemplo, griseofulvina y antibióticos, excepto amoxicilina y doxiciclina, que se ha demostrado que no afectan la liberación de hormonas de NuvaRing).
- El producto a base de hierbas llamado hierba de San Juan también puede afectar la eficacia de NuvaRing. Si desea utilizar productos que contengan hierba de San Juan mientras ya está usando NuvaRing, debe consultar primero a su médico.
- NuvaRing también puede interferir con el trabajo de otros medicamentos, como ciclosporina y el antiepiléptico lamotrigina.
Se pueden usar almohadillas absorbentes mientras se usa el NuvaRing. Inserte el NuvaRing antes de insertar la almohadilla. Se debe tener especial cuidado al retirar la almohadilla para asegurarse de que el anillo no se salga accidentalmente. Si esto ocurriera, simplemente lave el anillo en agua fría o tibia y vuelva a colocarlo inmediatamente.
El uso de productos espermicidas o de levadura vaginal no reduce la eficacia anticonceptiva de NuvaRing.
Advertencias Es importante saber que:
Niños y adolescentes
No se ha estudiado la seguridad y eficacia de NuvaRing en adolescentes menores de 18 años.
Pruebas de laboratorio
Si le van a realizar análisis de sangre u orina, informe a su profesional sanitario que está utilizando NuvaRing, ya que puede alterar los resultados de algunos análisis.
Embarazo y lactancia
NuvaRing no debe utilizarse si está embarazada o se sospecha que puede estarlo. Si queda embarazada mientras usa NuvaRing, debe quitarse el anillo y comunicarse con su médico.
Si desea dejar de usar NuvaRing porque quiere quedarse embarazada, consulte la sección "Cuándo desea dejar de usar NuvaRing".
No se recomienda NuvaRing durante la lactancia. Si desea utilizar NuvaRing durante la lactancia, consulte con su médico.
Conducción y uso de máquinas
Es poco probable que NuvaRing afecte a su capacidad para conducir o utilizar máquinas.
Posología y forma de empleo Modo de empleo Nuvaring: Posología
Usted mismo insertará el NuvaRing en la vagina y se lo quitará. Su médico le indicará cuándo empezar a usar NuvaRing por primera vez. El anillo vaginal debe insertarse el día apropiado del ciclo menstrual (ver la sección "Cuándo comenzar con el primer anillo") y dejarse en la vagina durante 3 semanas seguidas. Es una buena práctica verificar regularmente si el anillo todavía está en la vagina. Después de la tercera semana, quítese el NuvaRing y tómese una semana de descanso. Por lo general, el ciclo menstrual ocurrirá durante este intervalo sin anillo.
Cómo insertar y quitar NuvaRing
- Antes de insertar el anillo, compruebe que no haya caducado (consulte "Conservación de NuvaRing").
- Lávese las manos antes de insertar o quitar el anillo.
- Elija la posición que le resulte más cómoda, como estar de pie con una pierna levantada, en cuclillas o acostado.
- Saque NuvaRing de su sobre.
- Sostenga el anillo entre el pulgar y el índice, apriételo e insértelo suavemente en su vagina. Una vez que se haya insertado NuvaRing, no debería escuchar nada. Si siente alguna molestia, empuje suavemente NuvaRing hacia el interior de su vagina. La posición exacta del anillo dentro de la vagina no es importante.
- Después de 3 semanas, retire NuvaRing de la vagina. El NuvaRing se puede quitar enganchando el dedo índice debajo del borde frontal del anillo o agarrando el borde del anillo y tirando hacia afuera (ver Figura 5). Si encuentra el anillo en su vagina pero no puede quitarlo, debe contactar tu doctor.
- El anillo usado debe desecharse con la basura doméstica normal, preferiblemente dentro de la bolsa resellable. No tire NuvaRing por el inodoro.
Tres semanas con el anillo insertado, una semana sin
- A partir del día en que se inserta, el anillo vaginal debe mantenerse en la vagina sin interrupción durante 3 semanas.
- Después de 3 semanas, retire el anillo el mismo día de la semana en que se insertó, aproximadamente a la misma hora. Por ejemplo, si el NuvaRing se inserta un miércoles alrededor de las 10 pm, el anillo debe retirarse el miércoles del tercer día. la semana siguiente., alrededor de las 10 pm.
- Después de la extracción, no use el anillo durante 1 semana. El sangrado vaginal debe ocurrir durante esta semana. Por lo general, comienza 2-3 días después de la extracción de NuvaRing.
- Comience con un nuevo anillo exactamente después del intervalo de 1 semana (nuevamente el mismo día de la semana y aproximadamente a la misma hora) incluso si el sangrado vaginal aún no ha terminado. Si el nuevo anillo se inserta más de 3 horas después, la protección contra el embarazo puede verse reducida. En este caso, siga las instrucciones proporcionadas en el párrafo "Qué hacer si ... Olvidas insertar un nuevo anillo después de un intervalo sin anillo ".
Si usa NuvaRing como se describe anteriormente, el sangrado vaginal se producirá todos los meses aproximadamente en los mismos días.
Cuando empezar con el primer timbre
- Si no ha utilizado un anticonceptivo hormonal en el último mes
El primer NuvaRing debe insertarse el primer día de su ciclo natural (es decir, el primer día de su ciclo menstrual). NuvaRing comienza a ejercer su efecto de inmediato. No es necesario tomar otras medidas anticonceptivas.
Se permite comenzar con NuvaRing entre el día 2 y el día 5, pero si tiene relaciones sexuales en los primeros 7 días de usar NuvaRing, asegúrese de que también está usando un método anticonceptivo adicional (por ejemplo, un condón). Este consejo solo debe seguirse cuando utilice NuvaRing por primera vez.
- Si ha usado un anticonceptivo oral combinado (píldora) en el último mes
Comience a usar NuvaRing a más tardar el día después de la interrupción de la píldora actual sin píldoras. Si su paquete también contiene tabletas inactivas, comience a usar NuvaRing el día después de la última tableta inactiva a más tardar. Si no está seguro de cuál es, consulte a su médico o farmacéutico. Nunca extienda el intervalo libre de hormonas de su paquete de píldoras actual más allá de la longitud recomendada.
Si ha usado la píldora de manera constante y correcta y si está segura de que no está embarazada, también puede dejar de tomar la píldora cualquier día del paquete actual y comenzar a usar NuvaRing inmediatamente.
- Si ha utilizado un parche transdérmico en el último mes.
Empiece a usar NuvaRing el día después de su intervalo habitual sin parche como muy tarde. Nunca extienda el intervalo sin parche más allá de la cantidad de tiempo recomendada.
Si ha usado el parche de manera constante y correcta y si está segura de que no está embarazada, también puede dejar de usar el parche cualquier día y comenzar a usar NuvaRing inmediatamente.
- Si ha usado una píldora de progestágeno solo (minipíldora) en el último mes
Puede dejar de tomar la minipíldora cualquier día y comenzar a usar NuvaRing al día siguiente a la misma hora a la que normalmente hubiera tomado la píldora. Asegúrese de utilizar un método anticonceptivo adicional (por ejemplo, un condón) durante los primeros 7 días de uso del anillo.
- Si ha utilizado una inyección o un implante liberador de progestágeno o un DIU en el último mes
Empiece a usar NuvaRing el día de la nueva inyección o el día de la extracción del implante o del anillo del DIU liberador de progestágenos.
- Después de dar a luz
Si acaba de tener un bebé, su médico le indicará que espere su primer ciclo natural antes de comenzar a usar NuvaRing. En algunos casos, es posible comenzar antes. Pida consejo a su médico. Incluso si desea usar NuvaRing durante la lactancia, consulte primero a su médico.
- Después de un aborto natural o quirúrgico
Consulte a su médico.
Qué hacer si ...
El anillo se expulsa accidentalmente de la vagina.
NuvaRing puede salir accidentalmente de la vagina si, por ejemplo, no se ha insertado correctamente, durante la extracción de un tampón, durante las relaciones sexuales, junto con estreñimiento o prolapso del útero. Por lo tanto, debe verificar regularmente si el anillo está todavía en la vagina.
Si el anillo se deja fuera de la vagina por menos de 3 horas, aún la protegerá del embarazo. Enjuague el anillo con agua fría o tibia (no caliente) y vuelva a colocarlo. Si el anillo se deja fuera de la vagina durante más de 3 horas, es posible que no la proteja del embarazo. Consulte la información en "Qué hacer si ... El anillo está temporalmente fuera de la vagina".
El anillo permanece temporalmente fuera de la vagina.
Cuando está en la vagina, NuvaRing libera lentamente hormonas en el cuerpo para prevenir el embarazo. Si el anillo permanece fuera de la vagina durante más de 3 horas, es posible que no la proteja del embarazo, por lo que el anillo no debe permanecer fuera de la vagina durante más de 3 horas en un período de 24 horas.
- Si el anillo ha estado fuera de la vagina durante menos de 3 horas, aún puede protegerla del embarazo. Vuelva a insertar el anillo lo antes posible, pero a más tardar dentro de las 3 horas.
- Si el anillo permanece fuera de la vagina o sospecha que ha estado fuera de la vagina durante más de 3 horas durante la 1ª y 2ª semana, es posible que no la proteja del embarazo. Recuerde hacer esto y dejar el anillo en la vagina sin interrupción durante al menos 7 días.Use condón si tiene relaciones sexuales durante estos 7 días. Si se encuentra en la 1ª semana y ha tenido relaciones sexuales en los 7 días anteriores, existe la posibilidad de que esté embarazada, de ser así, póngase en contacto con su médico.
- Si el anillo permanece fuera de la vagina o sospecha que ha estado fuera de la vagina durante más de 3 horas durante la tercera semana, es posible que no la proteja del embarazo. Deseche ese anillo y elija una de las siguientes dos opciones:
- inserte un anillo nuevo inmediatamente. Esto iniciará el período de uso de las próximas 3 semanas. Es posible que el ciclo menstrual no aparezca, pero pueden producirse manchado o sangrado intermenstrual.
- No vuelva a insertar el anillo. Espere hasta que le llegue el período primero e inserte un nuevo anillo a más tardar 7 días después de que se haya quitado o haya salido el anillo anterior. Esta opción solo debe elegirse si NuvaRing se ha utilizado continuamente durante el período anterior. 7 días.
El anillo se rompe El NuvaRing rara vez se puede romper.
Si nota que el NuvaRing se ha roto, deseche ese anillo y comience con un nuevo anillo lo antes posible. Utilice precauciones anticonceptivas adicionales (por ejemplo, un condón) durante los próximos 7 días. Si ha tenido relaciones sexuales antes, notó la rotura del anillo. anillo, consulte a su médico.
Se ha insertado más de un anillo
No ha habido informes de efectos adversos graves por una sobredosis de hormonas NuvaRing. Si ha insertado accidentalmente más de un anillo, es posible que tenga náuseas, vómitos o sangrado vaginal. Retire el exceso de anillos y consulte a su médico si estos síntomas persisten. Olvidó ponerse un anillo nuevo después de un intervalo sin anillo Si el intervalo sin anillo es de más de 7 días, inserte un anillo nuevo tan pronto como se acuerde. Utilice también otro método anticonceptivo (por ejemplo, condón), si tiene relaciones sexuales , durante los próximos 7 días Si ha tenido relaciones sexuales durante el período de interrupción, se debe considerar la posibilidad de embarazo. Hable con su médico de inmediato. Cuanto más largo sea el intervalo sin anillo, mayor será el riesgo de embarazo.
Te olvidas de quitarte el anillo
- Si su anillo ha estado en su lugar por más de 3 pero no más de 4 semanas. Todavía puede protegerla del embarazo. Tome el intervalo regular sin anillo de una semana y luego inserte un anillo nuevo.
- Si su anillo se ha insertado durante más de 4 semanas, existe la posibilidad de embarazo. Comuníquese con su médico antes de insertar un nuevo anillo.
No hay menstruación
- NuvaRing se utilizó como se indica en las instrucciones.
Si ha perdido su período, pero NuvaRing se ha utilizado correctamente de acuerdo con las instrucciones y no ha tomado ningún otro medicamento, es muy poco probable que esté embarazada. Continúe usando NuvaRing como de costumbre. Sin embargo, si el período no ocurre dos veces seguidas, es posible que esté embarazada. Consulte a su médico de inmediato. No comience con un nuevo NuvaRing hasta que su médico haya descartado un embarazo.
- NuvaRing no se utilizó según lo recomendado
Si ha perdido su período y no ha seguido las instrucciones proporcionadas y no ha tenido su período esperado durante el próximo intervalo sin anillo, puede estar embarazada. Comuníquese con su médico antes de comenzar a usar un nuevo NuvaRing.
Tiene sangrado inesperado
Mientras usan NuvaRing, algunas mujeres pueden experimentar sangrado vaginal inesperado entre períodos. Puede ser necesario utilizar protección higiénica. En cualquier caso, deje el anillo en la vagina y continúe usándolo con normalidad.Consulte a su médico si el sangrado irregular persiste, se intensifica o se repite.
Quieres cambiar el primer día de tu ciclo menstrual
Si usa NuvaRing según las indicaciones, su ciclo menstrual (sangrado por privación) comenzará durante el intervalo sin anillo. Si desea cambiar el día de inicio de su período, puede acortar el intervalo sin anillo (¡nunca alargue este intervalo!)
Por ejemplo, si su período generalmente comienza un viernes, puede cambiar al martes (3 días antes) a partir del mes siguiente. Simplemente inserte el siguiente NuvaRing 3 días antes de lo habitual.
Si su intervalo sin anillo es muy corto (por ejemplo, 3 días o menos), es posible que no tenga su sangrado habitual, pero puede tener manchado (gotas o manchas de sangre) o sangrado intermenstrual mientras usa el siguiente anillo.
Si no está seguro de cómo proceder, comuníquese con su médico para obtener una aclaración.
Quieres posponer tu periodo
Aunque no es recomendable, es posible posponer la menstruación (hemorragia por deprivación) insertando un nuevo anillo inmediatamente después de retirar el anterior, sin tomar ningún intervalo libre de anillo. El nuevo anillo puede permanecer insertado hasta por 3 semanas. Mientras usa el nuevo anillo, puede experimentar manchado (gotas o manchas de sangre) o sangrado intermenstrual. Quítese el anillo cuando decida que quiere tener su período. Respete el intervalo normal sin anillo de una semana y luego inserte un anillo nuevo.
Puede pedirle consejo a su médico antes de decidir retrasar su período.
Cuándo quiere dejar de usar Nuvaring
Puede dejar de usar NuvaRing cuando lo desee.
Si no quiere quedar embarazada, consulte a su médico para conocer otros métodos anticonceptivos.
Si deja de usar NuvaRing porque desea quedar embarazada, debe esperar a que su ciclo natural comience antes de intentar concebir, lo que le ayudará a calcular su fecha de nacimiento prevista.
Efectos secundarios ¿Cuáles son los efectos secundarios de Nuvaring?
Como todos los medicamentos, NuvaRing puede producir efectos adversos, aunque no todas las personas los sufran.
Si experimenta algún efecto secundario, especialmente si es grave o persistente, o si hay algún cambio en su salud que cree que podría deberse a NuvaRing, informe a su médico.
Todas las mujeres que toman anticonceptivos hormonales combinados presentan un mayor riesgo de desarrollar coágulos de sangre en las venas (tromboembolismo venoso (TEV)) o coágulos de sangre en las arterias (tromboembolismo arterial (TEA)). Para obtener información más detallada sobre los diferentes riesgos de "tomar anticonceptivos hormonales combinados, consulte la sección" Qué necesita saber antes de usar NuvaRing ".
Si es alérgico a cualquiera de los componentes de NuvaRing (hipersensibilidad), puede tener los siguientes síntomas (frecuencia no conocida): angioedema [hinchazón de la cara, lengua y / o garganta y / o dificultad para tragar] o urticaria asociada con la respiración dificultades. Si esto ocurre, quítese el NuvaRing y consulte a su médico de inmediato.
Se han informado los siguientes efectos secundarios durante el uso de NuvaRing:
Frecuentes: pueden afectar hasta 1 de cada 10 mujeres.
- dolor abdominal; sentirse enfermo (náuseas)
- micosis vaginal (por ejemplo, "Candida"); malestar vaginal debido al anillo, picazón en el área genital; secreciones vaginales
- dolor de cabeza o migraña; estado de ánimo deprimido; disminución de la libido
- dolores de pecho; dolor pélvico; menstruación dolorosa
- acné
- aumento de peso
- expulsión del anillo
Poco frecuentes: pueden afectar hasta 1 de cada 100 mujeres.
- alteraciones visuales; mareo
- abdomen hinchado; vómitos, diarrea o estreñimiento
- sentirse cansado, indispuesto o irritable; cambios de humor; cambios de humor
- exceso de líquido en los tejidos (edema)
- infección del tracto urinario o de la vejiga
- dificultad o dolor al orinar; fuerte necesidad de orinar; orinar con más frecuencia
- Problemas durante las relaciones sexuales, incluido el dolor, el sangrado o la sensación del anillo en la pareja.
- aumento de la presión arterial
- Apetito incrementado
- dolor de espalda; espasmos musculares; dolor en las piernas o los brazos
- sensibilidad cutánea reducida
- senos doloridos o agrandados; mastopatía fibroquística (quistes mamarios que pueden hincharse y causar dolor)
- inflamación del cuello uterino; pólipos cervicales (crecimientos en el cuello uterino); eyección del borde del cuello uterino (ectropión)
- cambios en su ciclo menstrual (por ejemplo, los períodos pueden ser abundantes, largos, irregulares o pueden detenerse por completo); trastornos en el área pélvica; síndrome premenstrual; espasmos del útero
- infecciones vaginales (fúngicas y bacterianas); ardor, mal olor, dolor, malestar o sequedad de la vagina o vulva
- pérdida de cabello, eccema, picazón, erupción o sofocos
- ruptura del anillo
Raras: pueden afectar hasta 1 de cada 1.000 mujeres.
- coágulos de sangre dañinos en una vena o arteria, por ejemplo: o en una pierna o pie (TVP) o pulmón (EP) o ataque cardíaco o accidente cerebrovascular o mini accidente cerebrovascular o síntomas temporales similares a los de "accidente cerebrovascular, conocido como isquemia transitoria ataque (AIT) o coágulos de sangre en el hígado, estómago / intestinos, riñones u ojos. Su probabilidad de desarrollar un coágulo de sangre puede ser mayor si tiene otras afecciones que aumentan este riesgo (ver la sección sobre afecciones que aumentan el riesgo de coágulos y los síntomas de un coágulo de sangre).
- secreción mamaria. Frecuencia no conocida (la frecuencia no puede estimarse a partir de los datos disponibles)
- cloasma (parches de piel de color marrón amarillento, particularmente en la cara)
- malestar en el pene de su pareja (como irritación, sarpullido, picazón). Se han notificado casos de cáncer de mama y de hígado en asociación con el uso de anticonceptivos hormonales combinados Para más información ver sección "Cánceres".
Notificación de efectos secundarios
Si experimenta cualquier efecto adverso, consulte a su médico o farmacéutico, incluido cualquier posible efecto adverso no mencionado en este prospecto. También puede notificar efectos secundarios directamente a través del sistema nacional de notificación en "https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse". Al notificar efectos secundarios, puede ayudar a proporcionar más información sobre la seguridad de este medicamento
Caducidad y retención
Conservar por debajo de 30 ° C. Almacene en el paquete original para proteger el dispositivo de la luz y la humedad.
No use NuvaRing si se le dispensó hace más de 4 meses. La fecha de dispensación se indica en la caja y el sobre.
No utilice NuvaRing después de la fecha de caducidad que aparece en la caja y el sobre.
No use NuvaRing si nota algún cambio en el color del anillo o cualquier otro signo visible de deterioro.
Deseche el anillo usado con la basura doméstica normal, preferiblemente en el sobre con cierre. NuvaRing no se debe tirar por el inodoro. Al igual que con otros medicamentos, no se deshaga de los anillos no utilizados o vencidos por los desagües ni a la basura. Pregúntele a su farmacéutico cómo deshacerse de los anillos sin usar que ya no usa. Esto ayudará a proteger el medio ambiente.
Contenido del envase e información adicional
Qué contiene NuvaRing
- Los ingredientes activos son: etonogestrel (11,7 mg) y etinilestradiol (2,7 mg)
- Los demás componentes son: copolímeros de etileno acetato de vinilo (28% y 9% de acetato de vinilo) (un tipo de plástico que no se disuelve en el cuerpo) y estearato de magnesio.
El etonogestrel y el etinilestradiol se liberan del anillo en cantidades diarias de 0,120 mg / día y 0,015 mg / día, respectivamente, durante un período de 3 semanas.
Aspecto de NuvaRing y contenido del envase
NuvaRing es un anillo flexible, transparente, incoloro o casi incoloro con un diámetro de 54 mm.
Cada anillo está contenido en una bolsa de aluminio resellable y empaquetada en una caja de cartón junto con este prospecto. Cada caja contiene 1 o 3 anillos. Es posible que no se comercialicen todos los tamaños de envases.
Prospecto fuente: AIFA (Agencia Italiana de Medicamentos). Contenido publicado en enero de 2016. Es posible que la información presente no esté actualizada.
Para tener acceso a la versión más actualizada, es recomendable acceder al sitio web de la AIFA (Agencia Italiana de Medicamentos). Descargo de responsabilidad e información útil.
01.0 NOMBRE DEL MEDICAMENTO
NUVARING 0.120 MG / 0.015 MG CADA 24 HORAS DISPOSITIVO VAGINAL
02.0 COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
NuvaRing contiene 11,7 mg de etonogestrel y 2,7 mg de etinilestradiol. El anillo libera etonogestrel y etinilestradiol en cantidades medias de 0,120 mg y 0,015 mg, respectivamente, cada 24 horas, durante un período de 3 semanas.
Para consultar la lista completa de excipientes, ver sección 6.1.
03.0 FORMA FARMACÉUTICA
Dispositivo vaginal.
NuvaRing es un anillo flexible, transparente, incoloro o casi incoloro con un diámetro exterior de 54 mm y un diámetro de sección transversal de 4 mm.
04.0 INFORMACIÓN CLÍNICA
04.1 Indicaciones terapéuticas
Anticoncepción.
NuvaRing está indicado para mujeres en edad fértil. Se ha demostrado seguridad y eficacia en mujeres de 18 a 40 años.
La decisión de prescribir NuvaRing debe tener en cuenta los factores de riesgo actuales de cada mujer, en particular los relacionados con la tromboembolia venosa (TEV) y la comparación entre el riesgo de TEV asociado con NuvaRing y el asociado con otros AHC (ver secciones 4.3 y 4.4).
04.2 Posología y forma de administración
Dosis
Para lograr la eficacia anticonceptiva, NuvaRing debe usarse según lo prescrito (consulte "Cómo usar NuvaRing" y "Cómo comenzar a usar NuvaRing").
Población pediátrica
No se ha estudiado la seguridad y eficacia de NuvaRing en adolescentes menores de 18 años.
Método de administración
CÓMO USAR NUVARING
La mujer puede insertar NuvaRing en la vagina directamente. El médico debe informar a la mujer sobre cómo insertar y quitar el NuvaRing. Para la inserción, la mujer debe elegir la posición que le resulte más cómoda, como estar de pie con una pierna levantada, en cuclillas o acostada. El NuvaRing debe comprimirse entre dos dedos e insertarse en la vagina hasta que alcance una posición cómoda. L "La posición exacta de NuvaRing en la vagina no afecta el efecto anticonceptivo del anillo (ver Figuras 1-4).
Una vez que se ha insertado el NuvaRing (consulte "Cómo empezar a usar NuvaRing"), se deja en la vagina continuamente durante 3 semanas. La mujer debe tener el buen hábito de comprobar periódicamente la presencia de NuvaRing. En el caso de que NuvaRing sea expulsado accidentalmente, la mujer debe seguir las instrucciones de la sección 4.2 "Qué hacer si el" anillo se expulsa temporalmente de la vagina "(para más información, ver también la sección 4.4" Expulsión ").
NuvaRing debe retirarse después de 3 semanas de uso, el mismo día de la semana en que se colocó. Después de un intervalo sin anillo de una semana, se puede insertar un nuevo anillo (por ejemplo, si el NuvaRing se inserta un miércoles alrededor de las 10 pm, el anillo debe retirarse nuevamente el miércoles de la tercera semana siguiente, aproximadamente a las 10 pm. Se debe insertar un nuevo anillo el miércoles siguiente). NuvaRing se puede quitar enganchando el dedo índice debajo del anillo o agarrando el anillo entre los dedos índice y medio y tirando hacia afuera (Figura 5). El anillo usado debe colocarse en el sobre (manténgalo fuera del alcance de los niños y las mascotas) y desecharse como se describe en la sección 6.6. El sangrado por privación generalmente comienza 2-3 días después de que se retira NuvaRing y puede no terminar por completo cuando se retira el anillo nuevo. para ser insertado.
CÓMO EMPEZAR A USAR NUVARING
Sin tratamiento anticonceptivo hormonal en el ciclo anterior
NuvaRing debe insertarse el primer día del ciclo natural de la mujer (es decir, el primer día de su sangrado menstrual). También es posible comenzar del 2 al 5 día del ciclo, pero durante el primer ciclo, en los primeros 7 días de uso de NuvaRing, se recomienda utilizar además un método de barrera.
Cambio de un anticonceptivo hormonal combinado
La mujer debe colocarse NuvaRing a más tardar el día siguiente al intervalo habitual sin comprimidos o sin parche o después del último comprimido de placebo del anticonceptivo hormonal combinado anterior.
Si la mujer ha utilizado su método anterior de forma constante y correcta y está razonablemente segura de que no está embarazada, también puede cambiar su anticonceptivo hormonal combinado anterior en cualquier día del ciclo.
El intervalo libre de hormonas del método anterior nunca debe extenderse más allá del período recomendado.
Cambio de un método de progestágeno solo (minipíldora, implante o inyección) o de un sistema intrauterino liberador de progestágeno (SIU)
La mujer puede cambiar de una minipíldora cualquier día (de un implante o SIU, el día de la extracción, de un anticonceptivo inyectable cuando es el momento de la nueva inyección), pero en todos los casos debe utilizar un método de barrera adicional en la primera 7 días de uso de NuvaRing.
Después de un aborto en el primer trimestre
La mujer puede empezar de inmediato. De esta forma, no son necesarias medidas anticonceptivas adicionales. En caso de que no desee comenzar de inmediato, la mujer debe seguir las instrucciones del apartado "Sin tratamiento anticonceptivo hormonal en el ciclo anterior". Mientras tanto, se debe recomendar el uso de un método anticonceptivo alternativo.
Después de un parto o un aborto en el segundo trimestre
Para la lactancia, ver sección 4.6.
Se debe aconsejar a la mujer que comience el tratamiento durante la cuarta semana después del parto o del aborto en el segundo trimestre. Si comienza más tarde, se debe recomendar a la mujer que utilice un método de barrera adicional durante los primeros 7 días de uso de Sin embargo, si ya ha tenido relaciones sexuales ocurrido, se debe descartar un embarazo o la mujer debe esperar hasta su primer período menstrual antes de comenzar el tratamiento con NuvaRing.
DESVIACIONES DE LA DOSIS RECOMENDADA
La eficacia anticonceptiva y el control del ciclo pueden verse comprometidos si la mujer no cumple con la posología recomendada. En caso de desviación, se deben dar los siguientes consejos para evitar la pérdida de la eficacia anticonceptiva:
• Qué hacer si se amplía el intervalo sin anillo
La mujer debe insertar un anillo nuevo tan pronto como se acuerde de hacerlo. También se debe usar un método de barrera, como un condón, durante los próximos 7 días. Si el coito tuvo lugar durante el período sin anillo, se debe considerar la posibilidad de embarazo. Cuanto más largo sea el intervalo sin anillo, mayor será el riesgo de embarazo.
• Qué hacer si el anillo se expulsa temporalmente de la vagina
NuvaRing debe dejarse en la vagina durante un período continuo de 3 semanas. Si el anillo se expulsa accidentalmente, se puede lavar con agua fría o tibia (no caliente) y se debe volver a colocar inmediatamente.
Si NuvaRing se deja fuera de la vagina durante menos de 3 horas, la eficacia anticonceptiva no se reduce. La mujer debe volver a insertar el anillo lo antes posible, pero a más tardar dentro de las 3 horas.
Si NuvaRing permanece fuera de la vagina, o se sospecha que ha permanecido fuera de la vagina durante más de 3 horas durante la 1ª o 2ª semana de uso, la eficacia anticonceptiva puede verse reducida. La mujer debe volver a insertar el anillo tan pronto como se acuerde. eso. Se debe utilizar un método de barrera, como un condón, hasta que NuvaRing haya estado en la vagina de forma continua durante 7 días. Cuanto más tiempo haya estado NuvaRing fuera de la vagina y cuanto más cerca esté este período del intervalo libre del anillo, mayor será el riesgo de embarazo.
Si NuvaRing ha estado fuera de la vagina, o se sospecha que ha estado fuera de la vagina durante más de 3 horas durante la tercera semana del período de uso de tres semanas, la eficacia anticonceptiva puede verse reducida. La mujer debe desechar ese anillo y elegir uno. de las siguientes dos posibilidades:
1. Inserte inmediatamente un anillo nuevo
Nota: La inserción de un anillo nuevo iniciará el período de uso de las próximas tres semanas. Es posible que la mujer no tenga una hemorragia por deprivación de su ciclo anterior. Sin embargo, pueden producirse manchado o hemorragia intermenstrual.
2. Tener una hemorragia por deprivación e insertar un anillo nuevo a más tardar 7 días (7 x 24 horas) desde el momento en que se quitó o expulsó el anillo anterior.
Nota: Esta opción solo debe elegirse si el anillo se ha utilizado de forma continua durante los 7 días anteriores.
• Qué hacer en caso de uso prolongado del anillo
Aunque no es la posología recomendada, la eficacia anticonceptiva sigue siendo satisfactoria siempre que se haya utilizado NuvaRing durante un máximo de 4 semanas. La mujer puede mantener su intervalo de una semana sin anillo y luego insertar un nuevo anillo.Si el NuvaRing se ha insertado durante más de 4 semanas, la eficacia anticonceptiva puede verse reducida y debe descartarse la posibilidad de embarazo antes de insertar un nuevo NuvaRing.
Si la mujer no se ha adherido al régimen recomendado y posteriormente no se ha producido hemorragia por deprivación en el siguiente intervalo sin anillo, se debe descartar la posibilidad de embarazo antes de insertar un nuevo NuvaRing.
CÓMO MOVER O RETRASAR UN CICLO MENSTRUAL
Si, en casos excepcionales, es necesario retrasar un ciclo menstrual, la mujer puede insertar un nuevo anillo sin respetar ningún intervalo sin anillo. El siguiente anillo se puede usar hasta por 3 semanas más. La mujer puede tener sangrado vaginal o manchado. Luego, se reanuda el uso regular de NuvaRing después del intervalo habitual de una semana sin anillo.
Para cambiar su período a otro día de la semana que no sea el usado en su patrón actual, se le puede recomendar a la mujer que acorte su próximo intervalo sin anillo por la cantidad de días que prefiera. Cuanto más corto sea el intervalo sin anillo, mayor será el riesgo de que la mujer no tenga hemorragia por deprivación y pueda tener hemorragia intermenstrual y manchado durante el uso del siguiente anillo.
04.3 Contraindicaciones
Los anticonceptivos hormonales combinados (AOC) no deben usarse en las siguientes condiciones.
Si alguna de estas condiciones aparece por primera vez mientras usa el NuvaRing, debe quitarlo de inmediato.
• Presencia o riesgo de tromboembolismo venoso (TEV) o tromboembolismo venoso: TEV actual (con anticoagulante) o previo (p. Ej., Trombosis venosa profunda [TVP] o embolia pulmonar [EP])
• Predisposición hereditaria o adquirida conocida al tromboembolismo venoso, como resistencia a la proteína C activada (incluido el factor V Leiden), deficiencia de antitrombina III, deficiencia de proteína C, deficiencia de proteína S
• Cirugía mayor con inmovilización prolongada (ver sección 4.4)
• Alto riesgo de tromboembolismo venoso debido a la presencia de múltiples factores de riesgo (ver sección 4.4).
• Presencia o riesgo de tromboembolismo arterial (ATE) o tromboembolismo arterial: tromboembolismo arterial actual o previo (por ejemplo, infarto de miocardio) o condiciones prodrómicas (por ejemplo, angina de pecho)
• Enfermedad cerebrovascular: accidente cerebrovascular actual o previo o afecciones prodrómicas (p. Ej., Ataque isquémico transitorio (ataque isquémico transitorio, TIA))
• Predisposición hereditaria o adquirida conocida a la tromboembolia arterial, como hiperhomocisteinemia y anticuerpos antifosfolípidos (anticuerpos anticardiolipina, anticoagulante lúpico)
• Historia de migraña con síntomas neurológicos focales
• Un alto riesgo de tromboembolismo arterial debido a la presencia de múltiples factores de riesgo (ver sección 4.4) o la presencia de un factor de riesgo grave como:
• diabetes mellitus con síntomas vasculares
• hipertensión severa
• dislipoproteinemia severa.
• Pancreatitis o antecedentes de esta afección si se asocia con hipertrigliceridemia grave.
• Enfermedad hepática grave previa o actual hasta que los valores de la función hepática hayan vuelto a la normalidad.
• Tumores hepáticos (benignos o malignos), actuales o pasados.
• Enfermedades malignas conocidas o sospechadas de los órganos genitales o de las mamas, si son dependientes de hormonas.
• Sangrado vaginal de naturaleza desconocida.
• Hipersensibilidad a los principios activos oa alguno de los excipientes incluidos en la sección 6.1 de NuvaRing.
04.4 Advertencias especiales y precauciones de uso apropiadas
ADVERTENCIAS
Si se presenta alguna de las afecciones o factores de riesgo que se mencionan a continuación, se debe discutir con la mujer la idoneidad de NuvaRing.
En caso de que alguno de estos factores o condiciones de riesgo empeore o aparezca por primera vez, la mujer debe comunicarse con su médico para determinar si se debe suspender el uso de NuvaRing.
1. Trastornos circulatorios
Riesgo de tromboembolismo venoso (TEV)
El uso de cualquier anticonceptivo hormonal combinado (AOC) resulta en un mayor riesgo de tromboembolismo venoso (TEV) en comparación con su no uso. Los productos que contienen levonorgestrel, norgestimato o noretisterona se asocian con un menor riesgo de TEV. El riesgo asociado con otros productos. como NuvaRing también puede ser doble. La decisión de utilizar un producto diferente a los asociados con un menor riesgo de TEV solo debe tomarse después de conversar con la mujer para asegurarse de que comprende el riesgo de TEV asociado con NuvaRing, la forma en que su los factores de riesgo actuales influyen en ese riesgo y el hecho de que el riesgo de desarrollar un TEV es mayor en el primer año de uso.También hay alguna evidencia de que el riesgo aumenta cuando se reanuda la toma de un AOC después de una pausa de 4 semanas o más.
Aproximadamente 2 de cada 10,000 mujeres que no usan un AHC y que no están embarazadas desarrollarán un TEV durante un período de un año. En una mujer soltera, sin embargo, el riesgo puede ser mucho mayor, dependiendo de sus factores de riesgo subyacentes (ver más abajo).
Se estima que de cada 10,000 mujeres que usan un AHC de dosis baja que contiene levonorgestrel, alrededor de 61 desarrollarán un TEV en un año. Hubo resultados inconsistentes sobre el riesgo de TEV asociado con NuvaRing en comparación con los AOC que contienen levonorgestrel (con estimaciones de riesgo relativo que van desde ningún aumento, RR = 0,96 hasta un aumento de casi el doble, RR = 1,90). Estos valores corresponden a aproximadamente 6-12 TEV por año para 10,000 mujeres que usan NuvaRing.
En ambos casos, el número de TEV por año es menor que el número esperado en mujeres embarazadas o en posparto.
El TEV puede ser fatal en el 1-2% de los casos.
Muy raramente, se han notificado casos de trombosis en usuarios de AHC en otros vasos sanguíneos, p. Ej., Venas y arterias hepáticas, mesentéricas, renales o retinianas.
Factores de riesgo de TEV
El riesgo de complicaciones tromboembólicas venosas en las usuarias de AHC puede aumentar sustancialmente si existen factores de riesgo adicionales, especialmente si hay más de un factor de riesgo (ver tabla).
NuvaRing está contraindicado si una mujer tiene múltiples factores de riesgo que aumentan su riesgo de trombosis venosa (ver sección 4.3). Si una mujer tiene más de un factor de riesgo, es posible que el aumento del riesgo sea mayor que la suma de los factores individuales; en este caso, se debe considerar su riesgo total de TEV. Si la relación beneficio-riesgo se considera negativa , no se debe prescribir un AHC (ver sección 4.3).
Tabla: Factores de riesgo de TEV
No hay acuerdo sobre el posible papel de las varices y la tromboflebitis superficial en la aparición y progresión de la trombosis venosa.
Debe tenerse en cuenta el aumento del riesgo de tromboembolismo durante el embarazo, especialmente durante el período de 6 semanas del puerperio (para obtener información sobre "Embarazo y lactancia", ver sección 4.6).
Síntomas de TEV (trombosis venosa profunda y embolia pulmonar)
Si se presentan síntomas de este tipo, las mujeres deben buscar atención médica inmediata e informarles que están tomando un AHC.
Los síntomas de la trombosis venosa profunda (TVP) pueden incluir:
• Hinchazón unilateral de la pierna y / o pie oa lo largo de una vena de la pierna;
• dolor o sensibilidad en la pierna que solo se puede sentir al estar de pie o al caminar;
• aumento de la sensación de calor en la pierna afectada; piel de la pierna enrojecida o descolorida.
Los síntomas de la embolia pulmonar (EP) pueden incluir:
• aparición repentina e inexplicable de dificultad para respirar y respiración rápida;
• tos repentina que puede estar asociada con hemoptisis;
• dolor agudo en el pecho;
• aturdimiento o mareos intensos;
• latidos cardíacos rápidos o irregulares.
Algunos de estos síntomas (como "falta de aire" y "tos") no son específicos y pueden malinterpretarse como eventos más comunes o menos graves (por ejemplo, infecciones del tracto respiratorio).
Otros signos de oclusión vascular pueden incluir: dolor repentino, hinchazón o decoloración azul pálido de una extremidad.
Si la oclusión tiene lugar en el ojo, los síntomas pueden variar desde visión borrosa indolora hasta pérdida de visión. A veces, la pérdida de la visión ocurre casi de inmediato.
Riesgo de tromboembolismo arterial (ATE)
Los estudios epidemiológicos han asociado el uso de AHC con un mayor riesgo de tromboembolismo arterial (infarto de miocardio) o de accidentes cerebrovasculares (p. Ej., Ataque isquémico transitorio, accidente cerebrovascular). Los eventos tromboembólicos arteriales pueden ser fatales.
Factores de riesgo de ATE
El riesgo de complicaciones tromboembólicas arteriales o de un accidente cerebrovascular en las usuarias de AHC aumenta en presencia de factores de riesgo (ver tabla). NuvaRing está contraindicado si una mujer tiene un factor de riesgo grave o múltiples factores de riesgo de TEA que aumentan su riesgo de trombosis arterial (ver sección 4.3). Si una mujer tiene más de un factor de riesgo, es posible que el aumento del riesgo sea mayor que la suma de los factores individuales; en este caso, se debe considerar su riesgo total. Si se cree que el balance beneficio-riesgo es negativo, No se debe prescribir un AHC (ver sección 4.3).
Tabla: Factores de riesgo de ATE
Síntomas de ATE
Si se presentan síntomas de este tipo, las mujeres deben Comuníquese con un profesional de la salud de inmediato e infórmele que está tomando un AHC.
Los síntomas del accidente cerebrovascular pueden incluir:
• entumecimiento o debilidad repentinos de la cara, el brazo o la pierna, especialmente en un lado del cuerpo;
• dificultad repentina para caminar, mareos, pérdida del equilibrio o la coordinación;
• confusión repentina, dificultad para hablar o comprender;
• dificultad repentina para ver con uno o ambos ojos;
• migraña repentina, intensa o prolongada sin causa conocida;
• pérdida del conocimiento o desmayos con o sin convulsiones.
Los síntomas temporales sugieren que se trata de un ataque isquémico transitorio (AIT).
Los síntomas del infarto de miocardio (IM) pueden incluir:
• dolor, malestar, presión, pesadez, sensación de opresión o plenitud en el pecho, brazo o debajo del esternón;
• malestar que se irradia a la espalda, mandíbula, garganta, brazos, estómago;
• sensación de plenitud, indigestión o asfixia;
• sudoración, náuseas, vómitos o mareos;
• debilidad extrema, ansiedad o dificultad para respirar;
• latidos cardíacos rápidos o irregulares.
En el caso de un TEV o ATE sospechado o confirmado, el CHC debe suspenderse. Se debe iniciar una anticoncepción adecuada debido a la teratogenicidad de la terapia anticoagulante (cumarinas).
2. Tumores
• Los estudios epidemiológicos indican que el uso prolongado de anticonceptivos orales es un factor de riesgo para el desarrollo de cáncer de cuello uterino en mujeres con virus del papiloma humano (VPH). Sin embargo, sigue habiendo incertidumbre en cuanto a cuánto influyen en este hallazgo los factores de confusión (p. Ej., Diferencias en el número de parejas sexuales o el uso de barreras anticonceptivas.) No hay datos epidemiológicos sobre el riesgo de cáncer de cuello uterino en usuarias de NuvaRing (consulte "Exámenes / visitas médicas").
• Un metanálisis de 54 estudios epidemiológicos encontró que las mujeres que actualmente usan AHC tienen un riesgo relativo ligeramente mayor (RR = 1,24) de que se les diagnostique cáncer de mama. El exceso de riesgo desaparece gradualmente durante los 10 años siguientes a la interrupción del tratamiento. Dado que el cáncer de mama es poco común en mujeres menores de 40 años, la cantidad de casos adicionales de cáncer de mama diagnosticados en mujeres que toman o que toman AHC recientemente es baja en comparación con el riesgo general de cáncer de mama. El cáncer de mama diagnosticado en usuarias de anticonceptivos orales tiende a estar menos avanzado clínicamente que el diagnosticado en mujeres que nunca han usado un anticonceptivo oral. Las observaciones sobre el aumento del riesgo pueden deberse a un diagnóstico precoz de cáncer de mama en mujeres que toman AOC, los efectos biológicos del mismo o una combinación de ambos factores.
• Rara vez se han notificado tumores hepáticos benignos y, incluso más raramente, tumores hepáticos malignos en mujeres que toman AHC. En casos aislados, estos tumores han provocado hemorragias intraabdominales potencialmente mortales. Por lo tanto, si una mujer que usa NuvaRing experimenta dolor abdominal superior intenso, agrandamiento del hígado o signos que sugieran hemorragia intraabdominal, se debe considerar la posibilidad de cáncer de hígado en el diagnóstico diferencial.
3. Otras condiciones
• Las mujeres con hipertrigliceridemia o antecedentes familiares de esta afección pueden tener un mayor riesgo de pancreatitis cuando toman anticonceptivos hormonales.
• Aunque se han informado pequeños aumentos de la presión arterial en muchas mujeres que toman anticonceptivos hormonales, los aumentos clínicamente relevantes son eventos raros. No se ha establecido una correlación clara entre el uso de anticonceptivos hormonales y la hipertensión clínica. Sin embargo, si se produce una hipertensión prolongada clínicamente significativa durante el uso de NuvaRing, el médico debe, como precaución, suspender el uso del anillo y tratar el anillo. Si procede. , se puede reanudar el uso de NuvaRing si se han alcanzado valores normales de presión arterial después del tratamiento antihipertensivo.
• Se ha informado la aparición o empeoramiento de las afecciones enumeradas a continuación tanto durante el embarazo como mientras se toman anticonceptivos hormonales, pero no hay evidencia definitiva con respecto a la correlación entre estas afecciones y los anticonceptivos hormonales: ictericia y / o picazón debido a colestasis, formación de cálculos biliares, porfiria, lupus eritematoso sistémico, síndrome urémico hemolítico, corea de Sydenham, herpes gestacional, hipoacusia por otosclerosis, angioedema (hereditario).
• Las alteraciones agudas o crónicas de la función hepática pueden requerir la suspensión del uso de NuvaRing hasta que los parámetros de la función hepática hayan vuelto a la normalidad. El regreso de la ictericia colestásica y / o el prurito colestásico, que se produjo durante el embarazo o durante el tratamiento previo con esteroides sexuales, requiere la suspensión del uso del anillo.
• Aunque los estrógenos y progestágenos pueden afectar la resistencia periférica a la insulina y la tolerancia a la glucosa, no existe evidencia de la necesidad de un ajuste de régimen en pacientes diabéticos que usan anticonceptivos hormonales.
• Se ha informado un empeoramiento de la enfermedad de Crohn y la colitis ulcerosa en asociación con el uso de anticonceptivos hormonales.
• Ocasionalmente puede aparecer cloasma, especialmente en mujeres con antecedentes de cloasma gravídico. Las mujeres con tendencia al cloasma deben evitar la exposición al sol o la radiación ultravioleta mientras usan NuvaRing.
• Si una mujer tiene alguna de las siguientes condiciones, es posible que no pueda insertar correctamente el NuvaRing o que pierda el anillo: prolapso del cuello uterino, cistocele y / o rectocele, estreñimiento severo o crónico.
En muy raras ocasiones, se han notificado casos de inserción inadvertida de NuvaRing en la uretra, que posiblemente acabe en la vejiga, por lo que, si se presentan síntomas de cistitis, se debe considerar la colocación incorrecta en el diagnóstico diferencial.
• Ocasionalmente se pueden producir casos de vaginitis mientras se usa NuvaRing No hay indicios de que la eficacia de NuvaRing se vea afectada por el tratamiento de la vaginitis, ni de que el uso de NuvaRing afecte el tratamiento de la vaginitis (ver sección 4.5).
• En muy raras ocasiones se ha informado que el anillo se ha adherido al tejido vaginal, lo que requiere su extracción por parte de un profesional de la salud capacitado.
EXÁMENES / VISITAS MÉDICAS
Antes de iniciar o reanudar el uso de NuvaRing, se debe realizar una historia clínica completa (incluidos los antecedentes familiares) y se debe descartar un embarazo. Se debe medir la presión arterial y realizar un examen clínico, guiado por las contraindicaciones (ver sección 4.3) y advertencias (ver sección 4.4). Es importante llamar la atención de la mujer sobre la información relacionada con la trombosis venosa o arterial, incluido el riesgo asociado con NuvaRing en comparación con otros AHC, síntomas de TEV y TEA, factores de riesgo conocidos y qué hacer en caso de de sospecha de trombosis.
También se debe advertir a la mujer de la necesidad de leer detenidamente el prospecto y seguir sus consejos. La frecuencia y el tipo de exámenes deben basarse en pautas establecidas y deben adaptarse a la mujer en particular.
Se debe advertir a las mujeres que los anticonceptivos hormonales no protegen contra las infecciones por VIH (SIDA) y otras enfermedades de transmisión sexual.
REDUCCIÓN DE LA EFICACIA
La eficacia de NuvaRing puede verse reducida si no se respeta la información proporcionada (sección 4.2) o cuando se toman otros medicamentos al mismo tiempo (sección 4.5).
DISMINUCIÓN DEL CONTROL DE CICLO
Puede producirse sangrado irregular (manchado o hemorragia intermenstrual) durante el uso de NuvaRing. Si se produce sangrado irregular después de ciclos regulares previos mientras se utiliza NuvaRing en la posología recomendada, se debe considerar una causa no hormonal y, para excluir tumores malignos o embarazo, se debe considerar apropiado Se deben implementar medidas de diagnóstico, que pueden incluir legrado.
En algunas mujeres, es posible que no se produzca hemorragia por deprivación durante el intervalo sin anillo. Si se ha utilizado NuvaRing de acuerdo con las instrucciones descritas en la sección 4.2, es poco probable que esté embarazada. Se ha utilizado correctamente o si faltan dos hemorragias por deprivación, Se debe descartar un embarazo antes de continuar usando NuvaRing.
EXPOSICION DE "HOMBRE TODO" ETINILESTRADIOLO Y TODO "ETONOGESTREL
No se ha examinado el grado y el posible papel farmacológico de la exposición de la pareja sexual masculina al etinilestradiol y al etonogestrel a través de la absorción del pene.
ROTURA DEL ANILLO
Se ha informado que en muy raras ocasiones el anillo NuvaRing se ha abierto durante el uso (ver sección 4.5). Se debe aconsejar a la mujer que se quite el anillo roto y se vuelva a insertar un nuevo anillo lo antes posible, y que utilice adicionalmente un método de barrera, como un condón, durante los próximos 7 días. Se debe considerar la posibilidad de embarazo y la mujer debe comuníquese con el médico.
EXPULSIÓN
Se ha informado que NuvaRing puede ser expulsado, por ejemplo, si el anillo no se ha insertado correctamente, al quitarse un tampón, durante el coito o si tiene estreñimiento severo o crónico. La expulsión prolongada puede provocar un fallo anticonceptivo y / o hemorragia intermenstrual. .
Por tanto, para garantizar la eficacia, se debe aconsejar a la mujer que compruebe periódicamente la presencia de NuvaRing.
Si NuvaRing se expulsa accidentalmente y se deja fuera de la vagina durante menos de 3 horas, la eficacia anticonceptiva no se reduce. La mujer debe lavar el anillo con agua fría o tibia (no caliente) y volver a colocarlo lo antes posible, pero a más tardar. por 3 horas.
Si NuvaRing ha estado fuera de la vagina, o se sospecha que ha estado fuera de la vagina durante más de 3 horas, la eficacia anticonceptiva puede verse reducida. En ese caso, el consejo dado en la sección 4.2 "Qué hacer si el anillo está expulsado temporalmente de la vagina ".
04.5 Interacciones con otros medicamentos y otras formas de interacción
INTERACCIONES CON OTROS MEDICAMENTOS
Las interacciones entre los anticonceptivos hormonales y otros medicamentos pueden provocar hemorragias intermenstruales y / o fallo anticonceptivo Las siguientes interacciones se han informado en la bibliografía.
Metabolismo hepático: Pueden producirse interacciones con medicamentos que inducen enzimas microsomales, dando lugar a un aumento del aclaramiento de hormonas sexuales (p. Ej., Fenitoína, fenobarbital, primidona, carbamazepina, rifampicina y posiblemente también oxcarbazepina, topiramato, felbamato, ritonavir, griseofulvina y productos que contengan St. John's). mosto).
Las mujeres en tratamiento con cualquiera de estos medicamentos deben utilizar temporalmente un método de barrera además de NuvaRing o elegir otro método anticonceptivo. Con medicamentos inductores de enzimas microsomales hepáticas, el método de barrera debe utilizarse durante todo el período de administración concomitante del medicamento y durante los 28 días posteriores a la interrupción.
Si la administración concomitante del fármaco continúa más allá del ciclo de 3 semanas de un anillo, el siguiente anillo debe insertarse inmediatamente sin observar el intervalo habitual sin anillo.
También se ha informado pérdida de la eficacia anticonceptiva con antibióticos, como penicilinas y tetraciclinas, pero el mecanismo de este efecto no se ha entendido bien. En un estudio farmacocinético de interacción, la administración oral de amoxicilina (875 mg, dos veces al día) o doxiciclina (200 mg el día 1, seguidos de 100 mg al día) durante 10 días mientras se usaba NuvaRing, no afectó significativamente la farmacocinética de etonogestrel y EE. Las mujeres en tratamiento con antibióticos (excepto amoxicilina y doxiciclina) deben usar un método de barrera hasta 7 días después de la interrupción. Si la administración concomitante del medicamento continúa más allá de las 3 semanas del ciclo de un anillo, el siguiente anillo debe insertarse inmediatamente sin observar el anillo habitual. -intervalo libre.
Según los datos farmacocinéticos, no se espera que los antifúngicos y espermicidas vaginales afecten a la eficacia anticonceptiva y la seguridad de NuvaRing. Durante el uso concomitante de pesarios antifúngicos, la posibilidad de rotura del anillo puede ser ligeramente mayor (ver párrafo 4.4 "Rotura del" anillo ") .
Los anticonceptivos hormonales pueden interferir con el metabolismo de otros medicamentos. En consecuencia, las concentraciones plasmáticas y tisulares pueden aumentar (por ejemplo, ciclosporina) o disminuir (por ejemplo, lamotrigina).
Se debe consultar la información de prescripción de medicamentos concomitantes para identificar posibles interacciones.
EXÁMENES DE LABORATORIO
El uso de esteroides anticonceptivos puede influir en los resultados de algunas pruebas de laboratorio, incluidos los parámetros bioquímicos de la función hepática, tiroidea, suprarrenal y renal, los niveles plasmáticos de proteínas transportadoras (por ejemplo, globulina transportadora de corticosteroides y globulina transportadora de hormonas sexuales), del lípido. / fracciones de lipoproteínas, parámetros del metabolismo de los carbohidratos, coagulación y fibrinólisis. Las variaciones generalmente se encuentran dentro de los límites de los valores normales de laboratorio.
INTERACCIONES CON ALMOHADILLAS ABSORBENTES
Los datos farmacocinéticos muestran que el uso de tampones no tiene ningún efecto sobre la absorción sistémica de las hormonas liberadas por NuvaRing. En raras ocasiones, el NuvaRing puede ser expulsado durante la extracción de un tampón (consulte los consejos en "Qué hacer si" el anillo se expulsa temporalmente de la vagina ").
04.6 Embarazo y lactancia
Fertilidad
NuvaRing está indicado para la prevención del embarazo. Si la mujer quiere dejar de usar NuvaRing porque quiere quedar embarazada, se recomienda esperar hasta que tenga un período natural antes de intentar concebir, ya que esto la ayudará a calcular cuándo nacerá el bebé.
El embarazo
NuvaRing no está indicado durante el embarazo. Si queda embarazada con NuvaRing en el lugar, el anillo debe ser retirado. Estudios epidemiológicos extensos no han revelado ningún aumento del riesgo de defectos congénitos en niños nacidos de mujeres que usaron AOC antes del embarazo, ni ha habido efectos teratogénicos en los casos en los que se usó un AOC inadvertidamente durante el embarazo temprano. .
Un estudio clínico en un pequeño número de mujeres ha demostrado que, a pesar de la administración intravaginal, las concentraciones intrauterinas de esteroides anticonceptivos con NuvaRing son similares a los niveles observados en usuarias de AOC (ver sección 5.2).
No se ha informado de experiencia clínica con los resultados de embarazos expuestos a NuvaRing.
Se debe tener en cuenta el aumento del riesgo de tromboembolismo en el período posparto cuando se reinicia NuvaRing (ver secciones 4.2 y 4.4).
Hora de la comida
La lactancia puede verse influenciada por los estrógenos, ya que pueden reducir la cantidad y cambiar la composición de la leche materna, por lo que se debe desaconsejar el uso de NuvaRing hasta que la madre haya completado el destete. Es posible que pequeñas cantidades de esteroides anticonceptivos y / o sus metabolitos se excreten en la leche, pero no hay evidencia de que esto afecte negativamente la salud del bebé.
04.7 Efectos sobre la capacidad para conducir y utilizar máquinas
Según el perfil farmacodinámico, NuvaRing tiene una influencia nula o insignificante sobre la capacidad para conducir o utilizar máquinas.
04.8 Efectos indeseables
Los efectos secundarios notificados con más frecuencia en los ensayos clínicos con NuvaRing fueron dolor de cabeza, infecciones vaginales y flujo vaginal, cada uno de los cuales informó el 5-6% de las mujeres.
Descripción de algunas reacciones adversas
Se ha observado un aumento del riesgo de acontecimientos trombóticos y tromboembólicos arteriales y venosos, incluyendo infarto de miocardio, accidente cerebrovascular, ataques isquémicos transitorios, trombosis venosa y embolia pulmonar en usuarios de AHC, y este riesgo se analiza con más detalle en la sección 4.4.
También se han notificado otras reacciones adversas en mujeres que utilizan AOC: estas reacciones se comentan con más detalle en la sección 4.4.
La siguiente tabla enumera las reacciones adversas a medicamentos notificadas en ensayos clínicos, estudios observacionales o uso posterior a la comercialización con NuvaRing. Para describir un determinado evento adverso, se enumera el término MedDRA más apropiado.
Todas las reacciones adversas se enumeran por sistema de clasificación de órganos y frecuencia; frecuentes (≥ 1/100,
1) Lista de eventos adversos basada en informes espontáneos.
Se han notificado tumores dependientes de hormonas (p. Ej. Tumores de hígado, cáncer de mama) asociados con el uso de AOC (para más información, ver sección 4.4).
En raras ocasiones, las parejas de mujeres que utilizan NuvaRing han informado de enfermedades del pene durante la vigilancia posterior a la comercialización.
En mujeres que utilizan anticonceptivos hormonales combinados, se han informado varias reacciones adversas con más detalle en la sección 4.4. Estos efectos incluyen:
- trastornos tromboembólicos venosos;
- trastornos tromboembólicos arteriales;
- hipertensión;
- tumores dependientes de hormonas (por ejemplo, tumores de hígado, cáncer de mama);
- cloasma
Notificación de sospechas de reacciones adversas
La notificación de sospechas de reacciones adversas que se produzcan después de la autorización del medicamento es importante, ya que permite un seguimiento continuo de la relación beneficio / riesgo del medicamento. Se ruega a los profesionales sanitarios que notifiquen cualquier sospecha de reacciones adversas a través del sistema nacional de notificación. "Dirección:" www.agenziafarmaco.gov.it/it/responsabili ".
04.9 Sobredosis
No se han informado efectos adversos graves por sobredosis de anticonceptivos hormonales. En esta circunstancia pueden presentarse síntomas como náuseas, vómitos y, en las niñas, sangrado vaginal leve. No existen antídotos y cualquier tratamiento debe ser sintomático.
05.0 PROPIEDADES FARMACOLÓGICAS
05.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: Otros ginecológicos, anticonceptivos intravaginales, anillo vaginal con progestágeno y estrógeno, código ATC: G02BB01.
Mecanismo de acción
NuvaRing contiene etonogestrel y etinilestradiol. El etonogestrel es una progestina derivada de la 19-nortestosterona y se une con alta afinidad a los receptores de progesterona en los órganos diana. El etinilestradiol es un estrógeno muy utilizado en los anticonceptivos. El efecto anticonceptivo de NuvaRing se basa en varios mecanismos, el más importante de los cuales es la inhibición de la ovulación.
Eficacia clínica y seguridad
Se han realizado estudios clínicos en todo el mundo (EE. UU., Europa y Brasil) en mujeres de entre 18 y 40 años La eficacia anticonceptiva parece ser al menos comparable a la conocida para los anticonceptivos orales combinados. La siguiente tabla muestra los índices Pearl (número de embarazos por años de uso por 100 mujeres) encontrados en estudios clínicos con NuvaRing.
Con el uso de AOC en dosis más altas (0,05 mg de etinilestradiol) se reduce el riesgo de cáncer de endometrio y ovario.Queda por determinar si esto también se aplica a los anticonceptivos de dosis más bajas como NuvaRing.
PERFIL DE SANGRE
Un gran estudio comparativo versus un anticonceptivo oral levonorgestrel / etinilestradiol 150/30? G (n = 512 vs n = 518), que evaluó las características del sangrado vaginal durante 13 ciclos, mostró una baja incidencia de manchado o sangrado. (2,0-6,4%). Además, el sangrado vaginal se limitó exclusivamente al intervalo sin anillo en la mayoría de los sujetos (58,8% a 72,8%).
EFECTOS SOBRE LA DENSIDAD MINERAL HUESO
Los efectos de NuvaRing (n = 76) sobre la densidad mineral ósea se estudiaron en comparación con un dispositivo intrauterino no hormonal (DIU) (n = 31) durante un período de dos años. No se observaron efectos adversos sobre la masa ósea.
Población pediátrica
No se ha estudiado la seguridad y eficacia de NuvaRing en adolescentes menores de 18 años.
05.2 Propiedades farmacocinéticas
Etonogestrel
Absorción
El etonogestrel liberado por NuvaRing es rápidamente absorbido por la mucosa vaginal.Las concentraciones séricas máximas de etonogestrel, aproximadamente 1.700 pg / mL, se alcanzan aproximadamente una semana después de la inserción. Las concentraciones séricas muestran ligeras fluctuaciones y disminuyen lentamente a aproximadamente 1,600 pg / mL después de 1 semana, 1,500 pg / mL después de 2 semanas y 1,400 pg / mL después de 3 semanas de uso. La biodisponibilidad absoluta es aproximadamente del 100%, superior a la obtenida tras la administración oral. Se midieron los niveles de etonogestrel cervical e intrauterino en un pequeño número de mujeres que usaban NuvaRing o un anticonceptivo oral que contenía 0,150 mg de desogestrel y 0,020 mg de etinilestradiol. Los niveles observados fueron comparables.
Distribución
El etonogestrel se une a la albúmina sérica y a la globulina transportadora de hormonas sexuales (SHBG). El volumen aparente de distribución de etonogestrel es de 2,3 l / kg.
Biotransformación
El etonogestrel se metaboliza a través de vías conocidas de metabolismo de los esteroides. El aclaramiento sérico aparente es de aproximadamente 3,5 l / h. No se encontró interacción directa con etinilestradiol coadministrado.
Eliminación
Los niveles séricos de etonogestrel disminuyen de forma bifásica. La fase de eliminación terminal se caracteriza por una vida media de aproximadamente 29 horas. El etonogestrel y sus metabolitos se excretan en una relación orina / bilis de aproximadamente 1,7: 1. La vida media del metabolito de excreción es de aproximadamente 6 días.
Etinilestradiol
Absorción
El etinilestradiol liberado por NuvaRing es rápidamente absorbido por la mucosa vaginal. Las concentraciones séricas máximas, aproximadamente 35 pg / mL, se alcanzan 3 días después de la inserción y disminuyen a 19 pg / mL después de 1 semana, 18 pg / mL después de 2 semanas y 18 pg / mL después de 3 semanas de uso. La exposición sistémica mensual al etinilestradiol (AUC0-∞) con NuvaRing es de 10,9 ng • h / ml. La biodisponibilidad absoluta es aproximadamente del 56%, comparable a la ingesta oral de etinilestradiol. Se midieron los niveles de etinilestradiol cervical e intrauterino en un pequeño número de mujeres que usaban NuvaRing o un anticonceptivo oral que contenía 0,150 mg de desogestrel y 0,020 mg de etinilestradiol. Los niveles observados fueron comparables.
Distribución
El etinilestradiol se une en gran medida, pero no específicamente, a la albúmina sérica. Se determinó un volumen de distribución aparente de aproximadamente 15 L / kg.
Biotransformación
La principal vía metabólica del etinilestradiol es la hidroxilación aromática, pero también se forma una amplia variedad de metabolitos hidroxilados y metilados, presentes como metabolitos libres y como conjugados de sulfato y glucuronato. El aclaramiento aparente es de aproximadamente 35 L / h.
Eliminación
Los niveles séricos de etinilestradiol disminuyen de manera bifásica. La fase de eliminación terminal se caracteriza por una gran variación individual en la vida media que da como resultado una vida media de aproximadamente 34 horas. El etinilestradiol inalterado no se excreta; los metabolitos del etinilestradiol se excretan en una proporción orina / bilis de 1,3: 1. La vida media de excreción del metabolito es de aproximadamente 1,5 días.
Poblaciones especiales
Población pediátrica
No se ha estudiado la farmacocinética de NuvaRing en mujeres adolescentes sanas después de la menarquia menores de 18 años.
Efecto del daño renal
No se han realizado estudios para evaluar el efecto de la enfermedad renal en la farmacocinética de NuvaRing.
Efecto de la insuficiencia hepática
No se han realizado estudios para evaluar el efecto de la enfermedad hepática en la farmacocinética de NuvaRing, sin embargo, las hormonas esteroides pueden metabolizarse mal en mujeres con insuficiencia hepática.
Grupos étnicos
No se han realizado estudios formales para evaluar la farmacocinética en grupos étnicos.
05.3 Datos preclínicos sobre seguridad
Los datos de los estudios no clínicos con etinilestradiol y etonogestrel no muestran riesgos especiales para los seres humanos según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas, genotoxicidad, potencial carcinogénico y toxicidad para la reproducción, además de los ya conocidos para los seres humanos.
06.0 INFORMACIÓN FARMACÉUTICA
06.1 Excipientes
Copolímero de etileno acetato de vinilo, 28% de acetato de vinilo;
copolímero de etileno acetato de vinilo, 9% de acetato de vinilo;
estearato de magnesio.
06.2 Incompatibilidad
Irrelevante.
06.3 Período de validez
40 meses.
06.4 Precauciones especiales de conservación
Antes de dispensar:
3 años, conservar en nevera (entre 2 ° C y 8 ° C).
En el momento de la dispensación:
El farmacéutico escribe la fecha de venta en el paquete. El producto debe insertarse a más tardar 4 meses a partir de la fecha de venta, pero en cualquier caso antes de la fecha de vencimiento en caso de que ésta sea anterior.
Después de dispensar:
4 meses, conservar por debajo de 30 ° C.
Almacene en el paquete original para proteger el dispositivo de la luz y la humedad.
06.5 Naturaleza del envase primario y contenido del envase.
Sobre que contiene un solo NuvaRing. El sobre está fabricado con una lámina de aluminio cuya capa interior es de polietileno de baja densidad, mientras que la capa exterior es de tereftalato de polietileno (PET). El sobre es resellable e impermeable y está empaquetado en una caja de cartón impresa junto con el prospecto. Cada caja contiene 1 o 3 anillos.
Es posible que no se comercialicen todos los tamaños de envases.
06.6 Instrucciones de uso y manipulación
Ver sección 4.2. El farmacéutico debe indicar la fecha de venta en el paquete. Para el paquete de 3 anillos se recomienda indicar esta fecha en la caja exterior y en los sobres. NuvaRing debe insertarse a más tardar 4 meses a partir de la fecha de venta, pero en cualquier caso antes de la fecha de caducidad en caso de que sea anterior. .
07.0 TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
NEVADA. Organon
Kloosterstraat 6
5349 AB Obs
Países Bajos
08.0 NÚMERO DE AUTORIZACIÓN DE COMERCIALIZACIÓN
1 sobre que contiene 1 dispositivo vaginal
AIC N. 035584010
3 sobres cada uno con 1 dispositivo vaginal
AIC N. 035584022
09.0 FECHA DE LA PRIMERA AUTORIZACIÓN O RENOVACIÓN DE LA AUTORIZACIÓN
28 de mayo de 2002/1 de marzo de 2012
10.0 FECHA DE REVISIÓN DEL TEXTO
Julio de 2014











-inverno-2021-modelli-pi-belli.jpg)